12.下列有关原子结构和元素周期律表述正确的是( )
①ⅦA族元素是同周期中非金属性最强的元素
②原子序数为15的元素的最高化合价为+3
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族.
①ⅦA族元素是同周期中非金属性最强的元素
②原子序数为15的元素的最高化合价为+3
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族.
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ③④ |
11.下列事实不能用于判断元素金属性强弱的是( )
| A. | 金属间发生置换反应 | |
| B. | 金属元素的最高价氧化物对应水化物的碱性强弱 | |
| C. | 1mol金属单质在反应中失去电子的多少 | |
| D. | 金属元素的单质与水或酸反应置换出氢气的难易 |
10.下列有关元素周期表的说法正确的是( )
| A. | 第IA的元素全部是金属元素 | |
| B. | 元素周期表有18个族 | |
| C. | 元素周期表含元素最多的族是第ⅢB族 | |
| D. | 短周期是指第一、二、三、四周期 |
6.125℃时在容积不变的容器中:W、X、Y、Z的浓度变化如表:下列叙述中正确的是( )
| 物质 | W(g) | X(g) | Y(g) | Z(g) |
| 初始浓度(mol/L) | 4.0 | 2.0 | 0 | 0 |
| 2min末浓度(mol/L) | 2.4 | 1.2 | 0.8 | 1.6 |
| A. | 2min内X的平均速率为0.6mol/(L•min) | |
| B. | 该反应的化学方程式可表示为:2W(g)+X(g)?2Y+Z | |
| C. | 若达到平衡后保持压强不变充入Ne,平衡不移动 | |
| D. | 平衡后再加入W,则W的转化率增大 |
5.反应:2A(g)+3B(g)?C(g)+4D(g),速率最快的是( )
| A. | v(A)=2.0mol•L-1•min-1 | B. | v(B)=4.0mol•L-1•min-1 | ||
| C. | v(C)=0.1mol•L-1•s-1 | D. | v(D)=0.3mol•L-1•s-1 |
4.醋酸在水中电离方程式可表示为:CH3COOH?CH3COO-+H+△H>0,下列操作能使H+浓度增大的是( )
| A. | 加入少量NaOH固体 | B. | 加热升温10℃ | ||
| C. | 加入锌粉 | D. | 加入固体CH3COONa |
3.在一定温度下容积不变的容器中能说明反应:C(s)+H2O(g)?CO(g)+H2(g) 达到化学平衡状态的是( )
①气体的压强不变
②每生成n个CO分子同时生成n个H2分子
③四种物质的分子数之比为1:1:1:1
④气体的密度不变
⑤断裂2n个H-O键同时断裂n个H-H键
⑥气体的平均摩尔质量不变.
0 162737 162745 162751 162755 162761 162763 162767 162773 162775 162781 162787 162791 162793 162797 162803 162805 162811 162815 162817 162821 162823 162827 162829 162831 162832 162833 162835 162836 162837 162839 162841 162845 162847 162851 162853 162857 162863 162865 162871 162875 162877 162881 162887 162893 162895 162901 162905 162907 162913 162917 162923 162931 203614
①气体的压强不变
②每生成n个CO分子同时生成n个H2分子
③四种物质的分子数之比为1:1:1:1
④气体的密度不变
⑤断裂2n个H-O键同时断裂n个H-H键
⑥气体的平均摩尔质量不变.
| A. | ①④⑤⑥ | B. | ②⑤⑥ | C. | ①⑤⑥ | D. | ①②④⑤⑥ |
 .
.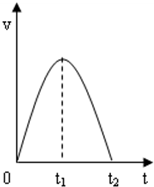 (1)将粉末形状大小相同的铁和铝分别与等浓度的稀盐酸反应产生气泡的速率铝>铁(填“<、>、=”).Al与盐酸反应的离子方程式是2Al+6H+=2Al3++3H2↑.
(1)将粉末形状大小相同的铁和铝分别与等浓度的稀盐酸反应产生气泡的速率铝>铁(填“<、>、=”).Al与盐酸反应的离子方程式是2Al+6H+=2Al3++3H2↑.