11.下列设计的实验方案与对应的现象或结论正确的是( )
| A. | 镁与水的反应实验:取一小段镁带,直接投入试管,向试管中加入2ml水并滴入2滴酚酞溶液,加热试管至沸腾,观察到溶液变红 | |
| B. | 为了确定酸碱中和是放热反应,实验中向10ml 2mol/L NaOH溶液中加入浓硫酸至恰好中和,测定出溶液温度升高 | |
| C. | 原电池能将化学能转化为电能:将锌片和铜片用导线连接(导线中间接入一个电流表),平行插入盛有稀硫酸溶液的烧杯中,观察到电流表指针偏转 | |
| D. | 探究不同催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLFeCl3溶液,向第二试管中加入2mL5%H2O2和少量MnO2粉末,不同的催化剂对化学反应速率的影响不同 |
10.航天飞船用高氯酸铵固体作燃料,点燃时的反应:2NH4ClO4$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+4H2O+Cl2↑+2O2↑.下列对该反应的叙述中不正确的是( )
| A. | 该反应中反应物的总能量小于生成物的总能量 | |
| B. | 该反应属于分解反应、氧化还原反应、放出能量的反应 | |
| C. | 高氯酸铵是一种盐,属于离子化合物 | |
| D. | 在能量变化上,该反应主要是化学能转变为热能和动能 |
9.2SO2(g)+O2(g)$?_{△}^{V_{2}O_{5}}$2SO3(g)是制备硫酸的重要反应.下列叙述正确的是( )
| A. | 催化剂V2O5不改变该反应的逆反应速率 | |
| B. | 增大压强,反应速率一定增大 | |
| C. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| D. | 在t1、t2时刻,SO3(g)的浓度分别是c1、c2(c1<c2),则时间间隔为 t1~t2内(t1<t2,以秒为单位),SO3(g)生成的平均速率为v=$\frac{({c}_{2}-{c}_{1})}{({t}_{2}-{t}_{1})}$ mol•L-1•s-1 |
8.下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 酸性HCl>H2S | 非金属性Cl>S |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | 向NaI溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈紫红色. | I-还原性强于Cl- |
| D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| A. | A | B. | B | C. | C | D. | D |
5.下列表示物质结构的化学用语或说法中,正确的是( )
| A. | 中子数为8的氮原子:${\;}_{8}^{15}$N | |
| B. | 次氯酸的电子式: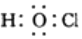 | |
| C. | PCl5分子的每个原子都满足8电子稳定结构 | |
| D. | 用电子式表示NaCl的形成过程: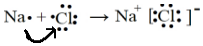 |
3.有如下合成路线,甲经二步转化为丙:
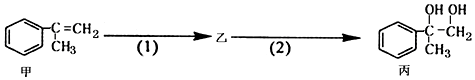
下列叙述错误的是( )
0 162678 162686 162692 162696 162702 162704 162708 162714 162716 162722 162728 162732 162734 162738 162744 162746 162752 162756 162758 162762 162764 162768 162770 162772 162773 162774 162776 162777 162778 162780 162782 162786 162788 162792 162794 162798 162804 162806 162812 162816 162818 162822 162828 162834 162836 162842 162846 162848 162854 162858 162864 162872 203614
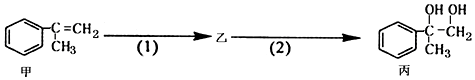
下列叙述错误的是( )
| A. | 物质丙能与氢氧化钠溶液反应 | |
| B. | 甲和丙均可使酸性KMnO4溶液褪色 | |
| C. | 反应(2)属于取代反应 | |
| D. | 步骤(2)产物中可能含有未反应的甲,可用溴水检验是否含甲 |
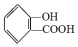 ,
,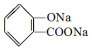 ;请写出将
;请写出将 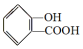 转化为
转化为 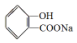 的化学方程式
的化学方程式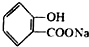 +H2O+CO2↑.
+H2O+CO2↑.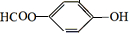
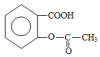 ,它与足量氢氧化钠溶液发生反应的方程式是
,它与足量氢氧化钠溶液发生反应的方程式是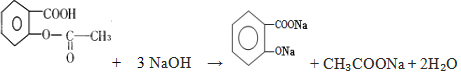 .
.