题目内容
7.应用元素周期律的有关知识,可以预测我们不熟悉的一些元素的单质及其化合物的性质.下列预测中正确的是( )①Be与Al的性质相似,所以其氧化物的水化物可能具有两性
②第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤Sr与Mg为同主族第五周期元素,SrSO4是难溶于水的白色固体
⑥Se为第四周期与氧同主族的元素,H2Se是无色、有毒、比H2S稳定的气体.
| A. | ①③⑤ | B. | ②④⑥ | C. | ①②③④ | D. | ②④⑤ |
分析 ①根据元素周期表中对角线规则知处于对角线的元素具有相似性;
②氨气溶于水显碱性;
③卤族元素单质从上到下,单质由气体过渡为固体,颜色逐渐加深,AgAt具有AgCl的相似的性质;
④Li燃烧生成Li2O,碱金属从上到下,金属性增强,最高价氧化物对应水化合物碱性增强;
⑤同主族元素化合物的性质具有相似性和递变性;
⑥元素的非金属性越强,其氢化物的稳定性越强.
解答 解:①元素周期表中Be和Al处于对角线位置上,处于对角线的元素具有相似性,所以Be的氧化物的水化物可能具有两性,故①正确;
②第二周期非金属元素的气态氢化物中氨气溶于水显碱性,甲烷难溶于水,故②错误;
③卤族元素单质从上到下,单质由气体过渡为固体,颜色逐渐加深,AgAt具有AgCl的相似的性质,不溶于水也不溶于稀硝酸,故③正确;
④Li燃烧生成Li2O,碱金属元素从上到下金属性增强,则LiOH为弱碱,故④错误;
⑤第ⅡA元素硫酸盐性质的递变规律,硫酸钡(BaSO4)是难溶于水的白色固体,则硫酸锶(SrSO4)是难溶于水的白色固体,故⑤正确;
⑥非金属性越强,气态氢化物越稳定,非金属性:S>Se,则氢化物稳定性为:H2S>H2Se,故⑥错误;
所以正确的有①③⑤,
故选A.
点评 本题考查同主族元素和同周期元素的性质变化规律以及对角线原则,为高频考点,侧重于基础知识的考查,题目难度不大,注意把握元素规律的运用.

练习册系列答案
相关题目
17.短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为 .请回答下列问题:
.请回答下列问题:
(1)Z元素位于元素周期表中第三周期VA族.
(2)X元素的最简单气态氢化物能与其最高价氧化物对应的水化物反应,得到的化合物属于离子化合物 (填“离子化合物”或“共价化合物”).
(3)X、Y、Z三种元素的原子半径由大到小的顺序为P>N>O(用元素符号表示).
(4)写出W单质与X的最高价氧化物对应水化物的浓溶液反应的化学方程式:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
 .请回答下列问题:
.请回答下列问题:| W | X | Y |
| Z |
(2)X元素的最简单气态氢化物能与其最高价氧化物对应的水化物反应,得到的化合物属于离子化合物 (填“离子化合物”或“共价化合物”).
(3)X、Y、Z三种元素的原子半径由大到小的顺序为P>N>O(用元素符号表示).
(4)写出W单质与X的最高价氧化物对应水化物的浓溶液反应的化学方程式:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
18.下列实验能达到预期目的是( )
| A. | 用溴水检验汽油中是否含有不饱和脂肪烃 | |
| B. | 除去苯中混有的苯酚,加入浓溴水,过滤 | |
| C. | 除去乙醇中混有的水,加入金属钠,蒸馏 | |
| D. | 乙烷气体中混有乙烯,通入酸性高锰酸钾溶液,洗气 |
15.利用人工光合作用合成甲酸的原理为2CO2+2H2O?2HCOOH+O2,装置如图所示,下列说法不正确的是( )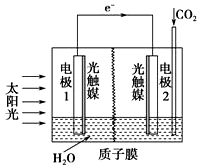

| A. | 该装置将太阳能转化为化学能和电能 | |
| B. | 电极1周围pH减小 | |
| C. | 电极2上发生的反应为CO2+2H++2e-═HCOOH | |
| D. | H+由电极2室经过质子膜流向电极1室 |
2.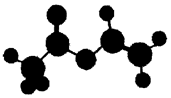 法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
 法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )| A. | 该化合物的名称为乙酸乙酯 | |
| B. | 该化合物与Br2的四氯化碳溶液不反应 | |
| C. | 该化合物既能发生水解反应,又能发生缩聚反应 | |
| D. | 该化合物的链状同分异构体中,能与NaHCO3反应放出CO2的只有3种 |
19.下列实验中,实验现象及结论都正确且两者具有因果关系的是( )
| 实验 | 现象 | 结论 | |
| A | 向Ba(NO3)2溶液中通入二氧化硫气体 | 有白色沉淀生成 | SO2与Ba(NO3)2反应得到BaSO3 |
| B | 向FeI2的溶液中滴加少量的氯水 | 溶液颜色变深 | Cl2与Fe2+反应生成Fe3+ |
| C | 向蔗糖溶液中加几滴稀硫酸,水浴加热5min后,再加新制Cu(OH)2后加热 | 无砖红色沉淀生成 | 蔗糖没有水解 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
16.足量的下列物质与相同质量的铝反应,放出氢气且消耗溶质物质的量最少的是( )
| A. | 稀硝酸 | B. | 稀硫酸 | C. | 盐酸 | D. | 氢氧化钠溶液• |