题目内容
3.有如下合成路线,甲经二步转化为丙: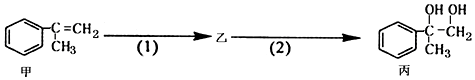
下列叙述错误的是( )
| A. | 物质丙能与氢氧化钠溶液反应 | |
| B. | 甲和丙均可使酸性KMnO4溶液褪色 | |
| C. | 反应(2)属于取代反应 | |
| D. | 步骤(2)产物中可能含有未反应的甲,可用溴水检验是否含甲 |
分析 由合成路线,甲经二步转化为丙,由C=C引入两个-OH,则反应(1)为C=C与卤素单质的加成反应,反应(2)为卤素原子的水解反应,以此来解答.
解答 解:A.丙不具有酸性,不能与氢氧化钠溶液反应,故A错误;
B.C=C、-OH均能被酸性KMnO4溶液氧化,则甲和丙均可与酸性KMnO4溶液发生反应,故B正确;
C.(2)属于卤代烃的水解反应,卤代烃的水解反应也属于取代反应,故C正确;
D.步骤(2)产物中可能含有未反应的甲,甲与溴水反应,而丙不能,则可用溴水检验是否含甲,故D正确.
故选A.
点评 本题考查有机物合成及结构与性质,为高频考点,把握合成反应中官能团的变化判断发生的反应为解答的关键,侧重烯烃、卤代烃、醇性质的考查,题目难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
13. 如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )
如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )
 如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )
如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )| A. | 与K+距离相等且最近的O2-有8个 | |
| B. | 与K+距离相等且最近的O2-构成的多面体是六面体 | |
| C. | 一个KO2晶胞中的K+和O2-的粒子数都是4个 | |
| D. | 与K+距离相等且最近的K+有8个 |
14.下列能够构成原电池的是( )
| A. | 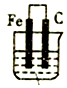 稀硫酸 | B. | 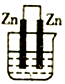 稀盐酸 | C. | 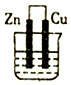 酒精 | D. | 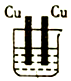 硫酸铜 |
11.下列关于阳离子的说法中错误的是( )
①阳离子都是由一个金属原子失去电子而形成的
②非金属原子不能形成阳离子
③阳离子的电子排布一定与稀有气体相同
④阳离子的价态不会大于其原子的最外层电子数
⑤阳离子都是稳定结构,不会再失去电子.
①阳离子都是由一个金属原子失去电子而形成的
②非金属原子不能形成阳离子
③阳离子的电子排布一定与稀有气体相同
④阳离子的价态不会大于其原子的最外层电子数
⑤阳离子都是稳定结构,不会再失去电子.
| A. | ①④ | B. | ②④ | C. | ①②③ | D. | ①②③④⑤ |
18.无放射性的同位素被称之为“稳定同位素”,在陆地生态系统研究中,2H、13C、15N、18O、34S等常作环境分析指示物.下列有关一些“稳定同位素”的说法错误的是( )
| A. | 34S原子核内中子数为18 | B. | 2H+的酸性比1H+的酸性更强 | ||
| C. | 16O与18O的化学性质几乎完全相同 | D. | 13C和15N原子核内的质子数相差1 |
8.下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 酸性HCl>H2S | 非金属性Cl>S |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | 向NaI溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈紫红色. | I-还原性强于Cl- |
| D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| A. | A | B. | B | C. | C | D. | D |
15. 用图装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
 用图装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| D | 液溴 | 苯 | 生成白雾 |
| A. | A | B. | B | C. | C | D. | D |
12.研究表明26Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是( )
| A. | 比较这两种元素的单质的硬度和熔点 | |
| B. | 向氯化铝和氯化镁的溶液中分别滴加过量的氢氧化钠溶液 | |
| C. | 使在空气中久置的镁带和铝片分别与热水作用,并滴入酚酞溶液 | |
| D. | 将铝片和镁片分别投入氢氧化钠溶液中,Al能与NaOH溶液反应放出氢气,而Mg不能 |