2.下列有关实验基本操作或现象的描述不正确的是( )
| A. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌 | |
| B. | 溶剂蒸发的速率越快,或浓缩后的溶液冷却得越快,析出的晶体颗粒就越大 | |
| C. | 油脂在热NaOH溶液中完全水解后加入饱和食盐水,可观察到液面上有固体析出 | |
| D. | 制备NaCl晶体时,晶体表面含有少量KNO3,用水淋洗后可得到较纯净的NaC1 |
1.下列操作能达到目的是( )
| A. | 将一块带有氧化膜的铝片与过量的浓NaOH溶液完全反应后,取澄清溶液将其蒸干,得纯净的NaAlO2固体 | |
| B. | 向NaAlO2溶液中加入过量的A1C13溶液,将所得沉淀过滤洗涤,加热灼烧去掉水分,可得纯净的A1(OH)3固体 | |
| C. | 把铝块与适量的稀盐酸完全反应,将所得溶液蒸干,可得AlCl3固体 | |
| D. | AlC3溶液与足量氨水反应,将沉淀过滤、洗涤、灼烧去掉水分可得Al2O3固体 |
20.下列分子式能表示的物质只有一种的是( )
| A. | C5H10 | B. | CH4O | C. | C7H8O | D. | C2H4Cl2 |
19.改变了“有机物就是有生命力的物质”观点的科学家是( )
| A. | 李比希 | B. | 维勒 | C. | 凯库勒 | D. | 诺贝尔 |
17.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.根据下表中短周期元素的原子半径和主要化合价,回答表后的问题.
(1)上述元素中与元素⑧处于同一周期的有Mg、P、Cl(填元素符号)
(2)元素①在元素周期表中的位置是第二周期ⅥA族
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为H2O>NH3>PH3(填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
③⑤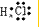 ②⑤
②⑤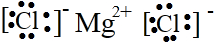 ③⑦
③⑦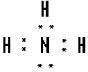
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:3H++Al(OH)3═Al3++3H2O.
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(2)元素①在元素周期表中的位置是第二周期ⅥA族
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为H2O>NH3>PH3(填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
③⑤
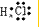 ②⑤
②⑤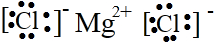 ③⑦
③⑦
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:3H++Al(OH)3═Al3++3H2O.
16.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 同主族元素性质的相似性 | 钠和氧反应可以形成Na2O2,也可以和硫形成Na2S2 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铁片分别加入足量的稀硫酸和浓硫酸中,浓硫酸中铁片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | H2O沸点低于H2S |
| D | 较强酸可以制取较弱酸 | 亚硫酸和次氯酸钙反应可以制取次氯酸 |
| A. | A | B. | B | C. | C | D. | D |
15.下列各组顺序的排列不正确的是( )
| A. | 熔点:金刚石>干冰 | B. | 离子半径:O2->Na+ | ||
| C. | 碱性:KOH>Al(OH)3 | D. | 稳定性:SiH4>H2S |
14.下列变化需克服共价键的是( )
| A. | 干冰受热变成二氧化碳气体 | B. | 金刚石熔化 | ||
| C. | 蔗糖溶于水 | D. | 食盐溶于水 |
13.化学与社会、生活和生产息息相关,以下叙述不正确的是 ( )
0 162673 162681 162687 162691 162697 162699 162703 162709 162711 162717 162723 162727 162729 162733 162739 162741 162747 162751 162753 162757 162759 162763 162765 162767 162768 162769 162771 162772 162773 162775 162777 162781 162783 162787 162789 162793 162799 162801 162807 162811 162813 162817 162823 162829 162831 162837 162841 162843 162849 162853 162859 162867 203614
| A. | 氢气的燃烧产物是水,是理想的清洁燃料,未来可以利用蓝绿藻和微生物制备氢气 | |
| B. | 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 | |
| C. | 生物炼铜的原理是利用某些具有特殊本领的细菌把不溶性的硫化铜转化为硫酸铜 | |
| D. | 硅晶体的导电性介于导体与绝缘体之间,是一种重要的半导体材料,广泛应用于制造集成电路、太阳能电池板等 |
