题目内容
15.下列各组顺序的排列不正确的是( )| A. | 熔点:金刚石>干冰 | B. | 离子半径:O2->Na+ | ||
| C. | 碱性:KOH>Al(OH)3 | D. | 稳定性:SiH4>H2S |
分析 A.干冰为二氧化碳固体,属于分子晶体,分子晶体的沸点小于原子晶体;
B.两种离子的电子层相同,核电荷数越大,离子半径越小;
C.金属性越强,最高价氧化物对应水合物的碱性越强;
D.非金属性越强,对应氢化物的稳定性越强.
解答 解:A.金刚石属于原子晶体,干冰为分子晶体,则熔点:金刚石>干冰,故A正确;
B.O2-、Na+都含有2个电子层,氧离子的核电荷数较小,其离子半径较大,则离子半径大小为:O2->Na+,故B正确;
C.金属性:K>Al,则最高价氧化物对应水合物的碱性:KOH>Al(OH)3,故C正确;
D.非金属性:Si<S,非金属性越强对应氢化物越稳定,则氢化物的稳定性:SiH4<H2S,故D错误;
故选D.
点评 本题考查原子结构与元素周期律的关系,题目难度不大,明确元素周期律的内容为解答关键,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
10.自热诗篇已成为现代生活的时尚.自热食品包装中有两包发热剂,在这两包发热剂中最适合盛饭的物质是( )
| A. | 熟石灰和水 | B. | 生石灰和水 | ||
| C. | 氯化钠和水 | D. | 氯化铵和氢氧化钡晶体 |
20.下列分子式能表示的物质只有一种的是( )
| A. | C5H10 | B. | CH4O | C. | C7H8O | D. | C2H4Cl2 |
7.不能作为判断氯、磷两种元素非金属性强弱的依据的是( )
| A. | 氧化性:Cl2>红磷 | B. | 单质沸点:红磷>C12 | ||
| C. | 氢化物稳定性:HC1>PH3 | D. | 酸性:HClO4>H3PO4 |
4.下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A. | 常温下遇铁都发生钝化 | B. | 常温下都能与铜反应产生氢气 | ||
| C. | 露置于空气中,溶液质量均不变 | D. | 露置于空气中,溶液浓度均不变 |
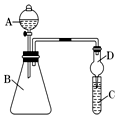 某学习小组同学利用如图装置来验证同主族元素非金属性的变化规律:
某学习小组同学利用如图装置来验证同主族元素非金属性的变化规律: