12.C和H2在生产、生活、科技中是重要的燃料.
①2C(s)+O2(g)═2CO(g)△H1=-220kJ/mol
②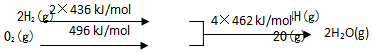
下列推断正确的是( )
①2C(s)+O2(g)═2CO(g)△H1=-220kJ/mol
②

下列推断正确的是( )
| A. | C(s)的燃烧热110 kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H1=+480 kJ/mol | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)△H1=+130 kJ/mol | |
| D. | 欲分解2 mol H2O(l),至少需要提供4×462 kJ 的热量 |
10.Na2CO3(aq)与盐酸反应过程中的能量变化示意图如图,下列选项正确的是( )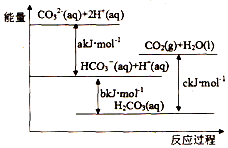

| A. | H2CO3(aq)=CO2(g)+H2O(l)为放热反应 | |
| B. | CO32-(aq)+H+(aq)=HCO3-(aq)△H=akJ/mol | |
| C. | HCO3-(aq)+H+(aq)=CO2(g)+H2O(l)△H=(c-b)kJ/mol | |
| D. | CO32-(aq)+2H+(aq)=CO2(g)+H2O(l)△H=(a+b-c)kJ/mol |
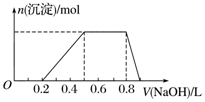
8.某溶液中可能含有下列5种离子中的某几种:Cl-、SO42-、SO32-、NH4+、Na+.为确认溶液组成进行如下实验:①向100mL上述溶液中加入足量BaCl2溶液,反应后将浊液过滤、洗涤、干燥,得沉淀4.50g,若向沉淀中加入过量的盐酸,仍有2.33g沉淀不溶.同时产生能使湿润红色石蕊试纸褪色的气体.②向①的滤液中加入足量的NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体0.56L(已换算成标准状况,假定产生的气体全部逸出).下列说法正确的是( )
| A. | 一定存在SO42-、SO32-、NH4+,可能存在Na+ | |
| B. | 一定存在SO42-、SO32-、NH4+,一定不存在Cl-、Na+ | |
| C. | 溶液中可能含有Cl-,且Na+浓度至少为0.15mol•L-1 | |
| D. | c(SO42-)=0.1mol•L-1,c(NH4+)<c(SO42-) |
7.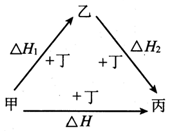 甲、乙、丙、丁四种物质在一 定条件下的转化关系如图所示,当乙作为反应物且与甲的物质的量相等时,△H=△H1+△H2.则甲、丙可能是( )
甲、乙、丙、丁四种物质在一 定条件下的转化关系如图所示,当乙作为反应物且与甲的物质的量相等时,△H=△H1+△H2.则甲、丙可能是( )
 甲、乙、丙、丁四种物质在一 定条件下的转化关系如图所示,当乙作为反应物且与甲的物质的量相等时,△H=△H1+△H2.则甲、丙可能是( )
甲、乙、丙、丁四种物质在一 定条件下的转化关系如图所示,当乙作为反应物且与甲的物质的量相等时,△H=△H1+△H2.则甲、丙可能是( )| A. | S、SO3 | B. | AlCl3、NaAlO2 | C. | Na、Na2O2 | D. | NaOH、Na2CO3 |
6. 研究发现,NOx和SO2是雾霾的主要成分,已知:
研究发现,NOx和SO2是雾霾的主要成分,已知:
2CO(g)+O2(g)?CO2(g)△H1=-566.00kJ•mol-1
2SO2(g)+O2(g)?2SO3(g)△H2=-196.6kJ•mol-1
2NO(g)+O2(g)?2NO2(g)△H3=-113.0kJ•mol-1
则反应2NO2(g)+SO2(g)+CO(g)?SO3(g)+2NO(g)+CO2(g)的△H=-268.3kJ•mol-1.NOx主要来源于汽车尾气.
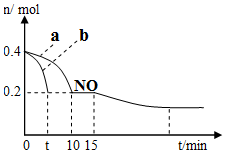
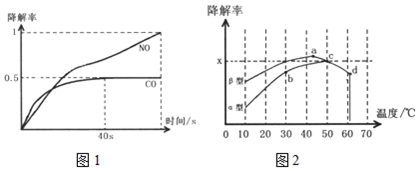
(1)T℃时,模拟汽车尾气催化转化:2NO+2CO?2CO2+N2,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化如图所示:
①T℃时该化学反应的平衡常数K=5(mol/L)-1;平衡时若保持温度不变,再向容器中充入0.2mol CO和0.4mol N2,平衡将向右移动.(填“向左”、“向右”或“不”)
②图1中a、b分别表示使用同种催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是b(填“a”或“b”).
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是增加CO的物质的量浓度或增大压强.
(二)SO2主要来源于煤的燃烧.
25℃时,电离平衡常数:
回答下列问题:
(2)①常温下,pH相同的下列溶液:I、Na2CO3,II、NaHCO3,III、Na2SO3.物质的量浓度由大到小的排列顺序为Ⅱ>Ⅲ>Ⅰ.(用序号表示)
②用纯碱溶液吸收SO2可将其转化为HSO3-,该反应的离子方程式是:H2O+2SO2+CO32-═2HSO3-+CO2↑.
(3)已知NaHSO3溶液显酸性,下列说法正确的是D.
A.c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3)
B.c(Na+)+c(H+)=c(OH─)+c(HSO3─)+c(SO32-)
C.c(HSO3-)>c(H+)>c(H2SO3)>c(SO32-)
D.c(H+)+c(H2SO3)=c(SO32-)+c(OH-)
 研究发现,NOx和SO2是雾霾的主要成分,已知:
研究发现,NOx和SO2是雾霾的主要成分,已知:2CO(g)+O2(g)?CO2(g)△H1=-566.00kJ•mol-1
2SO2(g)+O2(g)?2SO3(g)△H2=-196.6kJ•mol-1
2NO(g)+O2(g)?2NO2(g)△H3=-113.0kJ•mol-1
则反应2NO2(g)+SO2(g)+CO(g)?SO3(g)+2NO(g)+CO2(g)的△H=-268.3kJ•mol-1.NOx主要来源于汽车尾气.
(1)T℃时,模拟汽车尾气催化转化:2NO+2CO?2CO2+N2,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化如图所示:
①T℃时该化学反应的平衡常数K=5(mol/L)-1;平衡时若保持温度不变,再向容器中充入0.2mol CO和0.4mol N2,平衡将向右移动.(填“向左”、“向右”或“不”)
②图1中a、b分别表示使用同种催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是b(填“a”或“b”).
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是增加CO的物质的量浓度或增大压强.
(二)SO2主要来源于煤的燃烧.
25℃时,电离平衡常数:
| 化学式 | H2CO3 | H2SO3 |
| 电离平衡常数 | K1=4.30×10-7 K2=5.61×10-11 | K1=1.54×10-2 K2=1.02×10-7 |
(2)①常温下,pH相同的下列溶液:I、Na2CO3,II、NaHCO3,III、Na2SO3.物质的量浓度由大到小的排列顺序为Ⅱ>Ⅲ>Ⅰ.(用序号表示)
②用纯碱溶液吸收SO2可将其转化为HSO3-,该反应的离子方程式是:H2O+2SO2+CO32-═2HSO3-+CO2↑.
(3)已知NaHSO3溶液显酸性,下列说法正确的是D.
A.c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3)
B.c(Na+)+c(H+)=c(OH─)+c(HSO3─)+c(SO32-)
C.c(HSO3-)>c(H+)>c(H2SO3)>c(SO32-)
D.c(H+)+c(H2SO3)=c(SO32-)+c(OH-)
5.已知常温下0.1mol•L-1NH4HCO3溶液的pH=7.8.溶液中含氮(或含碳)各微粒的分布分数(平衡时某种 微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )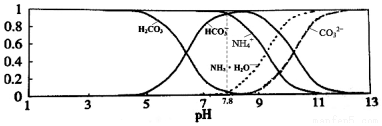

| A. | 当溶液的pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3-)>c(NH3•H2O)>c(CO32-) | |
| B. | 往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 | |
| C. | NH4HCO3溶液中:c(NH4+)+c(NH3•H2O)+c(H+)=c(CO32-)+c(H2CO3)+c(HCO3-)+c(OH-) | |
| D. | 通过分析可知常温下Kb(NH3•H2O)>Ka1(H2CO3) |
3.镁铝合金在碱性溶液中开始反应缓慢,后反应加快,经分析是氧化膜及微电池作用的结果.下列叙述正确的是( )
0 162668 162676 162682 162686 162692 162694 162698 162704 162706 162712 162718 162722 162724 162728 162734 162736 162742 162746 162748 162752 162754 162758 162760 162762 162763 162764 162766 162767 162768 162770 162772 162776 162778 162782 162784 162788 162794 162796 162802 162806 162808 162812 162818 162824 162826 162832 162836 162838 162844 162848 162854 162862 203614
| A. | 微电池的负极是Mg | B. | 微电池的负极是Al | ||
| C. | 铝的电极反应式为2H++2e-═H2↑ | D. | 镁的电极反应式为Mg-2e-═Mg2+ |
 ).
).