2.下列反应属于吸热反应的是( )
| A. | 钠与水反应 | B. | 甲烷在空气中燃烧 | ||
| C. | 盐酸与氢氧化钠溶液反应 | D. | 碳与二氧化碳高温反应 |
1.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 在50g质量分数为46%的乙醇水溶液中,含有氢原子数为3NA | |
| B. | 80℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | lmol有机物CH3-CH=CH-CH2-CH3中最多有9NA个原子在同一平面上 | |
| D. | l04g苯乙烯(C6H5-CH=CH2)中含有8NA的碳氢键和4NA的碳碳双键 |
19.五种短周期元素的某些性质如表所示,有关说法正确的是( )
| 元素 | 元素的相关信息 |
| M | 最高价氧化物对应水化物能与其气态氢化物反应生成盐 |
| W | 原子的M电子层上有3个电子 |
| X | 在短周期元素中,其原子半径最大 |
| Y | 最外层电子数是电子层数的2倍,且低价氧化物能与其气态氢化物反应生成Y的单质和H2O |
| Z | 元素最高正价与最低负价的代数和为6 |
| A. | M、Y、Z的简单离子半径依次增大 | |
| B. | W与Z形成的化合物属于离子化合物,其水溶液显酸性 | |
| C. | 化合物X2Y2、Y2Z2的晶体类型相同,化学键类型也相同 | |
| D. | M、W、X的最高价氧化物对应水化物两两之间能相互发生反应 |
18.下列设计的实验方案能达到实验目的是( )
| A. | 室温下,浓度均为0.1 mol•L-1Na2S2O3和H2SO4溶液,各取5 mL、10 mL的Na2S2O3溶液分别与10 mL的H2SO4溶液混合反应,验证Na2S2O3浓度对反应速率的影响 | |
| B. | 通过测定室温下等浓度的HNO3和H2SO4溶液的pH值,比较元素N、S的非金属性强弱 | |
| C. | KI--I2溶液中存在如下平衡:I2+I-?I3-.取V1mI平衡混合溶液,滴加几滴淀粉,用c mol/L的Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),滴定终点时消耗V2 mL的Na2S2O3溶液.根据V1、V2和c可测定上述平衡体系中c(I2) | |
| D. | 确定铝片中氧化铝的含量:取一定质量的铝片,与过量的NaOH溶液充分反应,溢出的气体通过硅胶后,冷却至室温后准确测量其体积 |
17.化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( )
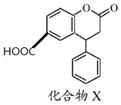

| A. | 分子中两个苯环一定处于同一平面 | |
| B. | 不能与饱和NaHCO3溶液反应 | |
| C. | 化合物X可以由 和 和 通过酯化反应得到 通过酯化反应得到 | |
| D. | 1 mol化合物X最多能与3 molNaOH反应 |
16. 短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径的大小:X<Y<Z<W | |
| B. | 元素的非金属性:Y>W>X | |
| C. | t中只含离子键 | |
| D. | v能抑制水的电离而u能促进水的电离 |
15.设NA为阿伏伽德罗常数的值.下列有关叙述正确的是( )
| A. | 硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA | |
| B. | 10g 46%的乙醇水溶液中所含氢原子数目为0.6NA | |
| C. | 标准状况下8.96L的平均相对分子质量为3.5的H2与D2含有中子数0.3NA | |
| D. | 1molCu与足量的S完全反应,转移电子数为2NA |
14.根据下列实验操作和现象所得结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 溴乙烷与NaOH乙醇溶液共热产生的气体通入KMnO4酸性溶液中,溶液褪色 | 产生的气体为乙烯 |
| B | 向浓度均为0.1mol•L-1的FeCl3和AlCl3混合溶液中滴加NaOH溶液,出现红褐色沉淀 | Ksp[Fe(OH)3]<Ksp[Al(OH)3] |
| C | 取少量淀粉水解液于试管中,加入过量氢氧化钠溶液和新制Cu(OH)2悬浊液,加热至沸腾,出现砖红色沉淀 | 淀粉已完全水解 |
| D | 在CuSO4溶液中加入KI溶液,再加入苯,振荡,有白色沉淀生成,苯层呈紫色 | 白色沉淀可能为CuI |
| A. | A | B. | B | C. | C | D. | D |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
0 162658 162666 162672 162676 162682 162684 162688 162694 162696 162702 162708 162712 162714 162718 162724 162726 162732 162736 162738 162742 162744 162748 162750 162752 162753 162754 162756 162757 162758 162760 162762 162766 162768 162772 162774 162778 162784 162786 162792 162796 162798 162802 162808 162814 162816 162822 162826 162828 162834 162838 162844 162852 203614
| A. | 27g铝中加入lmol/L的NaOH溶液,转移电子数是3NA | |
| B. | 56gN2与CO混合物中原子总数是4NA | |
| C. | 标准状况下,44.8LNO与22.4LO2反应后的分子数是2NA | |
| D. | 常温下,1LpH=l的H2SO4溶液中的H+为0.2NA |