题目内容
17.化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( )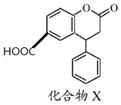
| A. | 分子中两个苯环一定处于同一平面 | |
| B. | 不能与饱和NaHCO3溶液反应 | |
| C. | 化合物X可以由 和 和 通过酯化反应得到 通过酯化反应得到 | |
| D. | 1 mol化合物X最多能与3 molNaOH反应 |
分析 有机物含有酯基,可发生水解反应,含有羧基,具有酸性,可发生中和、酯化反应,结合有机物的结构特点解答该题.
解答 解:A.两个苯环连接在饱和碳原子上,具有甲烷的结构特点,且C-C为δ键,可自由旋转,则分子中两个苯环不一定处于同一平面,故A错误;
B.含有羧基,可与饱和NaHCO3溶液反应,故B错误;
C.该化合物为内酯,由一种物质生成,故C错误;
D.能与氢氧化钠反应的为酯基、羧基,且酯基可水解生成酚羟基和羧基,则1 mol化合物X最多能与3 molNaOH反应,故D正确.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,题目难度中等,注意体会官能团与性质的关系,明确酸、酯的性质即可解答,试题培养了学生的灵活应用能力.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
8.理论上不能设计为原电池的化学反应是( )
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(l) | B. | HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l) | ||
| C. | 2H2(g)+O2(g)═2H2O(l) | D. | 2FeCl3(aq)+Fe(s)═3FeCl3(aq) |
5.二氧化氯(ClO2)是极易溶于水且不发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水.某小组在实验室中探究ClO2与Na2S的反应.回答下列问题:
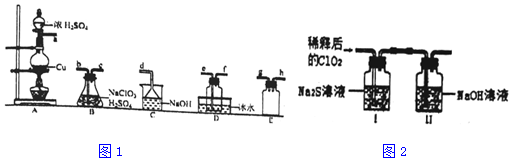
(1)ClO2的制备(已知SO2+2NaClO3+H2SO4═2ClO2↑+2NaHSO4)置A中反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
②欲收集干燥的ClO2,选择图1中的装置,其连接顺序为a→g→h→b→c→e→f→d(按气流方向,用小写字母表示)
③装置D的作用是冷凝并收集ClO2.
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图2所示装置中充分反应,得到无色澄清溶液.一段时间后,通过下列实验探究I中反应的产物.
④ClO2与Na2S反应的离子方程式为8ClO2+5S2-+4H2O=8Cl-+5SO42-+8H+.

(1)ClO2的制备(已知SO2+2NaClO3+H2SO4═2ClO2↑+2NaHSO4)置A中反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
②欲收集干燥的ClO2,选择图1中的装置,其连接顺序为a→g→h→b→c→e→f→d(按气流方向,用小写字母表示)
③装置D的作用是冷凝并收集ClO2.
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图2所示装置中充分反应,得到无色澄清溶液.一段时间后,通过下列实验探究I中反应的产物.
| 操作步骤 | 实验现象 | 结论 |
| 取少量I中溶液于试管甲中,滴加品红溶液和盐酸 | 品红始终不褪色 | ①无_SO2(或HSO3-或SO32-)生成 |
| 另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ②白色沉淀 | 有SO42- |
| ③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙中,________ | 有白色沉淀生成 | 有Cl-生成 |
12.将9.2g某芳香烃完全燃烧后的气体混合物通入过量的澄清石灰水中,石灰水共增重38g,然后过滤得到70g沉淀.已知该烃的相对原子质量小于100,下列说法不正确的是( )
| A. | 该烃的分子式为C7H8 | |
| B. | 该烃的含碳量大于乙烯的含碳量 | |
| C. | 该烃一氯代物有5种 | |
| D. | 该烃在光照或催化剂作用下能和氯气发生取代反应 |
2.下列反应属于吸热反应的是( )
| A. | 钠与水反应 | B. | 甲烷在空气中燃烧 | ||
| C. | 盐酸与氢氧化钠溶液反应 | D. | 碳与二氧化碳高温反应 |
9.分别处于第二、第三周期的主族元素A和B,它们的离子电子层结构相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B的原子序数分别是( )
| A. | m、n | B. | 3、7 | C. | m-2、10-n | D. | m+2、n+10 |
6.NA为阿伏加德罗常数的值.下列有关叙述正确的是( )
| A. | 标准状况下,2.24 L C12与足量铁粉反应转移的电子数为0.2NA | |
| B. | 2 L 0.1 mol•L-1Na2CO3溶液中所含CO32-的数目为0.2NA | |
| C. | 28 g C2H4所含共用电子对数目为4NA | |
| D. | 1 mol H2O中所含的中子数为10NA |
7.薄荷醇的结构简式如图,下列说法正确的是( )
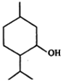

| A. | 薄荷醇分子中至少有12个碳原子共平面 | |
| B. | 薄荷醇分子式为C10H20O,它是环戊醇的同系物 | |
| C. | 1mol薄荷醇与足量NaHCO3反应生成22.4LCO2(标准状况) | |
| D. | 在一定条件下,薄荷醇能发生取代、中和、氧化等反应 |
 <
<