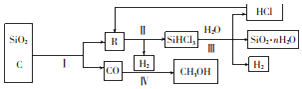
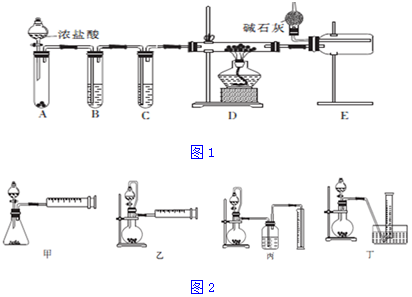
10.下列离子与氖原子核外电子排布不相同的是( )
| A. | Na+ | B. | F- | C. | Al3+ | D. | S2- |
9.已知某反应是放热反应,下列说法正确的是( )
| A. | 该反应中反应物的总能量大于生成物的总能量 | |
| B. | 该反应中反应物的总能量小于生成物的总能量 | |
| C. | 该反应发生时,一定不需要加热 | |
| D. | 如果该反应开始后停止加热,反应一定能继续进行 |
7.马日夫盐是一种白色晶体,易溶于水,常用于机械设备的磷化处理.以软锰矿(主要成分为MnO2,还含有少量的Fe2O3、FeO和Al2O3)为原料制备马日夫盐的流程如图:
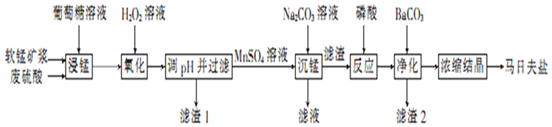
(1)软锰矿要先制成矿浆的目的是增大反应物接触面积,加快反应速率,提高原料利用率,葡萄糖(C6H12O6)与MnO2反应时,产物为MnSO4、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为12:1.
(2)用H2O2溶液“氧化”时发生反应的列子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如表所示、“调pH并过滤”时,应调整的pH范围为5.0~7.8,滤渣1的主要成分为Fe(OH)3和Al(OH)3(填化学式).
(4)加入磷酸后发生反应的化学方程式为MnCO3+2H3PO4═Mn(H2PO4)2+CO2↑+H2O.
(5)某工厂用上述流程制备马日夫盐,已知软锰矿中MnO2的含量为87%,整个流程中锰元素的损耗率为9%,则1t该软锰矿可制得马日夫盐2.5935t.

(1)软锰矿要先制成矿浆的目的是增大反应物接触面积,加快反应速率,提高原料利用率,葡萄糖(C6H12O6)与MnO2反应时,产物为MnSO4、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为12:1.
(2)用H2O2溶液“氧化”时发生反应的列子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如表所示、“调pH并过滤”时,应调整的pH范围为5.0~7.8,滤渣1的主要成分为Fe(OH)3和Al(OH)3(填化学式).
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.8 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
| Mn2+ | 7.8 | 9.8 |
(5)某工厂用上述流程制备马日夫盐,已知软锰矿中MnO2的含量为87%,整个流程中锰元素的损耗率为9%,则1t该软锰矿可制得马日夫盐2.5935t.
5.充分燃烧某烃的含氧衍生物,消耗氧气的体积与生成的二氧化碳的体积之比为9:8(相同条件下).则此有机物的最简通式是( )
| A. | Cn(H2O)m | B. | (C2O3)n(H2O)m | C. | (C2H)n(H2O)m | D. | (CO)n(H2O)m |
4.“类推”常用的学习方法,但有时会产生错误结论.下列类推的结论中,正确的是( )
| A. | IVA族元素氢化物沸点顺序是GeH4>SiH4>CH4,则VA族元素氢化物沸点顺序也是AsH3>PH3>NH3 | |
| B. | 常见的氢化物是分子晶体,则所有氧化物都是分子晶体 | |
| C. | 晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子 | |
| D. | 第二周期元素氢化物稳定性顺序是HF>H2O>NH3,则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3 |
3.在元素周期表中,原子最外电子层只有2个电子的元素是( )
| A. | 无法判断是哪一类元素 | B. | 一定是稀有气体元素 | ||
| C. | 一定是过渡元素 | D. | 一定是金属元素 |
2.下列说法都正确的是( )
①生活中使用频率很高的一元纸币将逐步被硬币替代,硬币是合金
②江河入海口三角洲的形成通常与胶体的性质有关
③“钡餐”中使用的硫酸钡是弱电解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和H2O2,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物.
①生活中使用频率很高的一元纸币将逐步被硬币替代,硬币是合金
②江河入海口三角洲的形成通常与胶体的性质有关
③“钡餐”中使用的硫酸钡是弱电解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和H2O2,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物.
| A. | ①②③④ | B. | ①②④⑥ | C. | ①②⑤⑥ | D. | ③④⑤⑥ |
1.阿司匹林(主要成分为乙酰水杨酸)是解热止痛、治疗感冒的药物.它是由水杨酸(邻羟基苯甲酸)与醋酸酐进行酯化反应制得的.其反应原理如下:
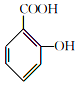 +
+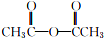 $→_{75-80℃}^{H_{3}PO_{4}}$
$→_{75-80℃}^{H_{3}PO_{4}}$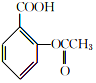 +CH3COOH
+CH3COOH
为避免醋酸酐水解,所用原料、仪器要充分干燥.有关物质的参数如表:
制取阿司匹林的工艺流程如下:
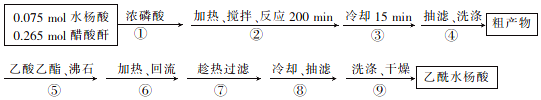
回答下列问题:
(1)浓磷酸的作用是催化剂.步骤②的加热方式为水浴加热,温度控制在75~80℃.
(2)向粗产物中加入乙酸乙酯的作用是溶解水杨酸和醋酸酐等杂质,同时减少乙酰水杨酸因溶解而造成的损失.
(3)验证最后得到的乙酰水杨酸产品较为纯净的方法是测定产品熔点.
(4)精制后乙酰水杨酸的质量为8.91g,则其产率为66%,造成产率低的原因可能有反应温度没有控制好(或粗产品回流时的温度过高,造成产品水解发生副反应等)(任写一点).
0 162646 162654 162660 162664 162670 162672 162676 162682 162684 162690 162696 162700 162702 162706 162712 162714 162720 162724 162726 162730 162732 162736 162738 162740 162741 162742 162744 162745 162746 162748 162750 162754 162756 162760 162762 162766 162772 162774 162780 162784 162786 162790 162796 162802 162804 162810 162814 162816 162822 162826 162832 162840 203614
 +
+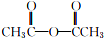 $→_{75-80℃}^{H_{3}PO_{4}}$
$→_{75-80℃}^{H_{3}PO_{4}}$ +CH3COOH
+CH3COOH为避免醋酸酐水解,所用原料、仪器要充分干燥.有关物质的参数如表:
| 名称 | 式量 | 性质 | 熔点/℃ | 沸点/℃ | 溶解度 | ||
| 水 | 乙醇 | 乙酸乙酯 | |||||
| 水杨酸 | 138 | 白色结晶粉末、无臭 | 157~159 | 211 | 溶 | 易溶 | 易溶 |
| 醋酸酐 | 102 | 无色液体、易燃、有醋酸味 | -73.1 | 138.6 | 易溶 | 溶 | 易溶 |
| 乙酸水杨酸 | 180 | 白色针状结晶 | 135 | 321.4 | 冰水微溶、热水可溶 | 易溶 | 微溶 |

回答下列问题:
(1)浓磷酸的作用是催化剂.步骤②的加热方式为水浴加热,温度控制在75~80℃.
(2)向粗产物中加入乙酸乙酯的作用是溶解水杨酸和醋酸酐等杂质,同时减少乙酰水杨酸因溶解而造成的损失.
(3)验证最后得到的乙酰水杨酸产品较为纯净的方法是测定产品熔点.
(4)精制后乙酰水杨酸的质量为8.91g,则其产率为66%,造成产率低的原因可能有反应温度没有控制好(或粗产品回流时的温度过高,造成产品水解发生副反应等)(任写一点).