3.A、B、C、D、E是五种元素,它们的核外电子排布如表所示:
(1)属于同一周期的元素是B、D、E(填元素符号,下同).
(2)属于同一主族的元素是A、C、E.
(3)B单质与水反应的化学反应方程式是2Na+2H2O=2NaOH+H2↑.
(4)E单质与水反应的化学反应方程式是Cl2+H2O=HCl+HClO.
| 元素 | 各电子层的电子数 | |||
| K | L | M | N | |
| A | 2 | 7 | ||
| B | 2 | 8 | 1 | |
| C | 2 | 8 | 18 | 7 |
| D | 2 | 8 | 2 | |
| E | 2 | 8 | 7 | |
(2)属于同一主族的元素是A、C、E.
(3)B单质与水反应的化学反应方程式是2Na+2H2O=2NaOH+H2↑.
(4)E单质与水反应的化学反应方程式是Cl2+H2O=HCl+HClO.
20.某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.
(1)该反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1mol•L-1)的用量均为2mL.在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
(2)计算用0.001mol•L-1KMnO4酸性溶液进行实验时KMnO4的平均反应速率1×10-4mol/(L•min)(忽略混合前后溶液的体积变化).
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?不行.(填“行”或“不行”)
0 162623 162631 162637 162641 162647 162649 162653 162659 162661 162667 162673 162677 162679 162683 162689 162691 162697 162701 162703 162707 162709 162713 162715 162717 162718 162719 162721 162722 162723 162725 162727 162731 162733 162737 162739 162743 162749 162751 162757 162761 162763 162767 162773 162779 162781 162787 162791 162793 162799 162803 162809 162817 203614
(1)该反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1mol•L-1)的用量均为2mL.在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
| KMnO4酸性溶液 的浓度/mol•L-1 | 溶液褪色所需时间t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?不行.(填“行”或“不行”)




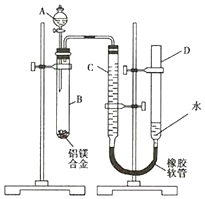 某学习小组用如图装置测定镁铝合金中铝的质量分数.
某学习小组用如图装置测定镁铝合金中铝的质量分数.
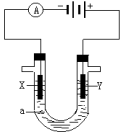 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.回答以下问题: