题目内容
20.某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.(1)该反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol•L-1、0.001mol•L-1,每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1mol•L-1)的用量均为2mL.在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
| KMnO4酸性溶液 的浓度/mol•L-1 | 溶液褪色所需时间t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?不行.(填“行”或“不行”)
分析 (1)高锰酸钾具有强氧化性,能将草酸氧化为二氧化碳,本身被还原为锰离子,据此书写离子方程式;
(2)先求出反应开始时c(KMnO4),然后求出三次褪色的平均时间,最后根据ν(KMnO4)=$\frac{△c}{△t}$进行计算;
(3)因颜色是由KMnO4产生,虽然KMnO4浓度大反应快,但KMnO4的量也多,故无法比较.
解答 解:(1)高锰酸钾具有强氧化性,能将草酸氧化为二氧化碳,本身被还原为锰离子,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(2)反应开始时:c(KMnO4)=$\frac{0.001mol/L×0.004L}{0.004L+0.002L}$=0.00067 mol•L-1
反应时间:△t=$\frac{6min+7min+7min}{3}$=6.7min
KMnO4的平均反应速率v(KMnO4)=$\frac{△c}{△t}$=$\frac{0.00067mol/L}{6.7min}$=1×10-4 mol/(L•min)
故答案为:1×10-4 mol/(L•min);
(3)由题中数据知浓度大的褪色时间反而长,因颜色是由KMnO4产生,虽然KMnO4浓度大反应快,但KMnO4的量也多,故无法比较,故不经过计算直接利用表中的褪色时间长短来判断浓度大小与反应速率的关系是不可行的,
故答案为:不行.
点评 本题考查了影响化学反应速率的因素,侧重于学生的分析、实验能力的考查,难度不大,熟练掌握外界条件对化学反应速率的影响为解答关键.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
6. 将两种两种气态烃组成的混合气体完全燃烧,得到CO2和H2O的物质量与混合烃的物质的置的关系如图所示.
将两种两种气态烃组成的混合气体完全燃烧,得到CO2和H2O的物质量与混合烃的物质的置的关系如图所示.
①一定有C2H4
②一定有CH4
③一定有C3H8
④一定没有C2H6
⑤可能有C2H2
⑥可能有C3H4
则上述对该混合烃的判断正确的是( )
 将两种两种气态烃组成的混合气体完全燃烧,得到CO2和H2O的物质量与混合烃的物质的置的关系如图所示.
将两种两种气态烃组成的混合气体完全燃烧,得到CO2和H2O的物质量与混合烃的物质的置的关系如图所示.①一定有C2H4
②一定有CH4
③一定有C3H8
④一定没有C2H6
⑤可能有C2H2
⑥可能有C3H4
则上述对该混合烃的判断正确的是( )
| A. | ②③⑤ | B. | ⑤⑥ | C. | ②④⑥ | D. | ①④ |
7.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 11.2 LNH3所含分子数为0.5NA | |
| B. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| C. | 23g金属钠与氧气加热生成Na2O2的反应,转移的电子数为2NA | |
| D. | 5.6g铁与足量的盐酸反应,失去的电子数为0.2NA |
8. (1)已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol
(1)已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol
H2(g)═H2(l),△H=-0.92kJ/mol
O2(g)═O2(l),△H=-6.84kJ/mol
请写出液氢和液氧生成气态水的热化学方程式H2(l)+$\frac{1}{2}$O2(l)=H2O(g)△H=-237.46KJ/mol
(2)氢气、氧气不仅燃烧时能释放热能,二者形成的原电池还能提供电能,美国的探月飞船“阿波罗号”使用的就是氢氧燃料电池,电解液为KOH溶液,正极发生的电极反应式为O2+4e-+2H2O=4OH-.
(3)一定温度下,在2L密闭容器中NO2和O2可发生下列反应:
4NO2(g)+O2(g)?2N2O5(g)
已知体系中n(NO2)随时间变化如表:
①写出该反应的平衡常数表达式:K=$\frac{{C}^{2}({N}_{2}{O}_{5})}{{C}^{4}(N{O}_{2})×C({O}_{2})}$,已知:K300℃>K350℃,则该反应是放热反应
②达到平衡后,NO2的转化率为49.6%,此时若再通入量氮气,则NO2的转化率将不变(填“增大”、“减小”、“不变”);
③右图中表示N2O5的浓度的变化曲线是c;
用O2表示从0~500s内该反应的平均速率v=1.51×10-3mol/(L•s).
 (1)已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol
(1)已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/molH2(g)═H2(l),△H=-0.92kJ/mol
O2(g)═O2(l),△H=-6.84kJ/mol
请写出液氢和液氧生成气态水的热化学方程式H2(l)+$\frac{1}{2}$O2(l)=H2O(g)△H=-237.46KJ/mol
(2)氢气、氧气不仅燃烧时能释放热能,二者形成的原电池还能提供电能,美国的探月飞船“阿波罗号”使用的就是氢氧燃料电池,电解液为KOH溶液,正极发生的电极反应式为O2+4e-+2H2O=4OH-.
(3)一定温度下,在2L密闭容器中NO2和O2可发生下列反应:
4NO2(g)+O2(g)?2N2O5(g)
已知体系中n(NO2)随时间变化如表:
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(ml) | 20 | 13.96 | 10.08 | 10.08 |
②达到平衡后,NO2的转化率为49.6%,此时若再通入量氮气,则NO2的转化率将不变(填“增大”、“减小”、“不变”);
③右图中表示N2O5的浓度的变化曲线是c;
用O2表示从0~500s内该反应的平均速率v=1.51×10-3mol/(L•s).
12.利用如图装置进行实验,下列有关实验操作和现象正确的是( )
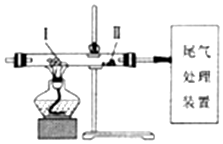

| A. | 缓慢通入N2,再加热Ⅰ处的碳酸氢钠,可观察到Ⅱ处过氧化钠粉末由浅黄色变成白色 | |
| B. | 缓慢通入N2,加热Ⅰ处KClO3和MnO2的混合物,可观察到Ⅱ处干燥KI淀粉试纸变成蓝色 | |
| C. | 先对Ⅰ处的氯化铵加热,再缓慢通入N2,可看到Ⅰ处固体减少,Ⅱ处无固体沉积 | |
| D. | 先缓慢通入CO2,再加热Ⅰ处炭粉,可观察到Ⅱ处氧化铁粉末由红色变成黑色 |
9.胶体与溶液的本质区别是( )
| A. | 是否属于混合物 | B. | 是否无色透明 | ||
| C. | 分散质粒子直径大小 | D. | 有无丁达尔效应 |
10.下列说法错误的是( )
| A. | 糖类、油脂和蛋白质均是高分子化合物 | |
| B. | 雾能产生丁达尔效应,雾属于胶体 | |
| C. | 新制氯水、HClO和SO2都有漂白作用 | |
| D. | 硝酸能与苯发生取代反应 |

