3.白磷分子(P4)为正四面体构型,其中P原子的杂化形式为( )
| A. | sp3 | B. | sp2 | C. | sp | D. | 不确定 |
2.反应 HF(aq)+BF3(aq)=H+(aq)+BF4-(aq) 能够发生的原因是( )
| A. | 强氧化剂制弱氧化剂 | B. | 强酸制弱酸 | ||
| C. | “熵增效应(熵判据)” | D. | 产物中形成了配位键 |
19.下列关于碱金属、卤族元素的说法正确的是( )
| A. | 碱金属单质的失电子能力随着原子序数的增加而减小 | |
| B. | 从上到下,卤素原子的电子层数依次增多,半径依次减小 | |
| C. | 从F到I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱 | |
| D. | 碱金属单质都是强氧化剂 |
18.将少量铝粉加入某溶液中有氢气放出,则该溶液中一定能大量共存的离子组是( )
| A. | K-、Ba2+、NO3-、SO32- | B. | NH4+、Al3+、Cl-、SO42- | ||
| C. | K Na2+[Al(OH)4]-、SO42- | D. | Na+、K+、SO42-、Br- |
17.下列有关金属及其合金的说法不正确的是( )
| A. | 目前我国流通的硬币是由合金材料制造的 | |
| B. | 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 | |
| C. | 出土的古代铜制品表面覆盖着铜绿其主要成分为 CuO | |
| D. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
16. 含乙酸钠和对氯酚(
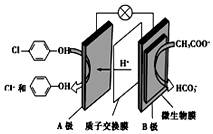
含乙酸钠和对氯酚(  )的废水可以利用微生物电池除去,其原理如图所示:下列说法正确的是( )
)的废水可以利用微生物电池除去,其原理如图所示:下列说法正确的是( )
 含乙酸钠和对氯酚(
含乙酸钠和对氯酚(  )的废水可以利用微生物电池除去,其原理如图所示:下列说法正确的是( )
)的废水可以利用微生物电池除去,其原理如图所示:下列说法正确的是( )| A. | B极是电解池的负极 | |
| B. | 电子从A极沿导线经小灯泡流向B极 | |
| C. | A极的电极反应式为: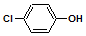 +e-═Cl-+ +e-═Cl-+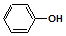 | |
| D. | 当外电路中有1 mol e-转移时,通过质子交换膜的H+为1 mol |
15.在恒温、密闭容器中投入一定量的CaCO3发生分解反应:CaCO3(s)?CaO(s)+CO2(g)△H>0达到平衡时,测得体系中气体的压强为P.若温度不变,缩小体积至原来的一半,重新达到平衡.下列说法的错误是( )
| A. | 当CaCO3的浓度不再变化时,表明达到平衡状态 | |
| B. | 重新达到新平衡时,CO2的压强为P | |
| C. | 扩大容器体积,重新达到平衡时n(CO2)增多 | |
| D. | 常温常压下CaCO3的分解反应不一定自发 |
14.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
0 162609 162617 162623 162627 162633 162635 162639 162645 162647 162653 162659 162663 162665 162669 162675 162677 162683 162687 162689 162693 162695 162699 162701 162703 162704 162705 162707 162708 162709 162711 162713 162717 162719 162723 162725 162729 162735 162737 162743 162747 162749 162753 162759 162765 162767 162773 162777 162779 162785 162789 162795 162803 203614
| A. | 乙酸和乳酸(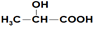 )的混合物共3.0 g,含有的原子总数为0.4 NA )的混合物共3.0 g,含有的原子总数为0.4 NA | |
| B. | 4.6 g乙醇含有-OH数为NA | |
| C. | 1.7 g H2O2中含有的电子数为NA | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
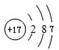 ;D微粒的核外电子排布式为1s2 2s22p6 3s23p6.
;D微粒的核外电子排布式为1s2 2s22p6 3s23p6.