题目内容
3.白磷分子(P4)为正四面体构型,其中P原子的杂化形式为( )| A. | sp3 | B. | sp2 | C. | sp | D. | 不确定 |
分析 根据分子中中心原子的价层电子对数判断杂化类型和分子的空间构型,分析解答.
解答 解:白磷分子(P4)为正四面体构型,结构为: ,每个磷与三个磷形成三个σ键,每个磷含有一对孤对电子对,所以要有四个杂化轨道,则P原子的杂化形式为sp3,故选A.
,每个磷与三个磷形成三个σ键,每个磷含有一对孤对电子对,所以要有四个杂化轨道,则P原子的杂化形式为sp3,故选A.
点评 本题考查原子杂化方式判断,明确价层电子对互斥理论是解本题关键,知道价层电子对个数的计算方法,为考试高频点,题目难度中等.

练习册系列答案
相关题目
11.下列溶液一定呈中性的是( )
| A. | 不含OH-的溶液 | B. | 使酚酞试剂呈无色的溶液 | ||
| C. | pH=7的溶液 | D. | c(H+)=$\sqrt{{K}_{w}}$的溶液 |
18.将少量铝粉加入某溶液中有氢气放出,则该溶液中一定能大量共存的离子组是( )
| A. | K-、Ba2+、NO3-、SO32- | B. | NH4+、Al3+、Cl-、SO42- | ||
| C. | K Na2+[Al(OH)4]-、SO42- | D. | Na+、K+、SO42-、Br- |
8.如图甲、乙是两种重要的有机合成原料.下列有关说法中,不正确的是( )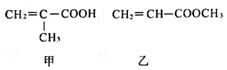
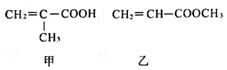
| A. | 甲与乙互为同分异构体 | |
| B. | 甲与乙都能与溴的四氯化碳溶液发生加成反应 | |
| C. | 甲与乙都能与金属钠反应产生氢气 | |
| D. | 在一定条件下,甲与乙均能发生取代反应 |
15.下列各组物质的晶体中,化学键类型和晶体类型均相同的是( )
| A. | NH3和HCl | B. | CO2和SiO2 | C. | Ar和Al | D. | CCl4和NH4Cl |
12.分类是学习和研究化学的一种重要方法.下列分类不合理的是( )
| A. | Na2SiO3和KHCO3都属于盐 | B. | KOH和NH3都属于碱 | ||
| C. | H2SO4和H2S都属于酸 | D. | CaO和NO都属于氧化物 |
13. 2015年,中国科学家屠哟哟因发现治疗疟疾的药物青蒿素获得了诺贝尔奖.青蒿素结构简式如图所示.己知一个碳原子上连有4个不同的原子或基团,该碳原子称了“手性碳原子”.下列有关青蒿素的说法不正确的是( )
2015年,中国科学家屠哟哟因发现治疗疟疾的药物青蒿素获得了诺贝尔奖.青蒿素结构简式如图所示.己知一个碳原子上连有4个不同的原子或基团,该碳原子称了“手性碳原子”.下列有关青蒿素的说法不正确的是( )
 2015年,中国科学家屠哟哟因发现治疗疟疾的药物青蒿素获得了诺贝尔奖.青蒿素结构简式如图所示.己知一个碳原子上连有4个不同的原子或基团,该碳原子称了“手性碳原子”.下列有关青蒿素的说法不正确的是( )
2015年,中国科学家屠哟哟因发现治疗疟疾的药物青蒿素获得了诺贝尔奖.青蒿素结构简式如图所示.己知一个碳原子上连有4个不同的原子或基团,该碳原子称了“手性碳原子”.下列有关青蒿素的说法不正确的是( )| A. | 青蒿素分子有6个手性碳原子 | |
| B. | 青蒿素的化学式为:C15H22O5 | |
| C. | 青蒿素在一定条件下能与NaOH溶液反应,且有氧化性 | |
| D. | 青蒿素难溶于水,提取的方法是用有机溶剂萃取后蒸馏 |