20.下列说法正确的是( )
| A. | SiO2不能与HNO3、H2SO4等所有的酸反应 | |
| B. | 由Na2CO3+SiO$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑可知硅酸的酸性比碳酸的酸性强 | |
| C. | 硅胶常用于做干燥剂 | |
| D. | CO2与SiO2均是酸性氧化物,溶于水均得到相应的酸 |
18. 汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:
汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:
2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.
(1)写出CO2的结构式O=C=O,N2的电子式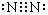 .
.
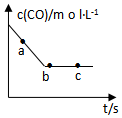
(2)一定条件下,在容积固定的容器中进行上述反应,CO浓度与时间关系如图所示:
①则反应速率υ(a)、υ(b)、υ(c)的大小关系是υ(a)>υ(b)=υ(c);
②下列可说明反应到达图中c点的是BC;
A.NO、CO、CO2、N2的浓度比值保持2:2:2:1不变
B.CO的浓度不再改变
C.反应消耗2molNO的同时消耗1molN2
D.容器中的气体质量或物质的量保持不变
(3)为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
【资料查阅】
A.不同的催化剂对同一反应的催化效率不同;
B.使用等质量相同的催化剂时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
【结论】①实验编号Ⅱ的实验目的为探究催化剂比表面积对反应速率的影响.
②课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是温度,且升高温度反应速率将增大.(填“增大”、“减小”、“无影响”).
 汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:
汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.
(1)写出CO2的结构式O=C=O,N2的电子式
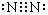 .
.(2)一定条件下,在容积固定的容器中进行上述反应,CO浓度与时间关系如图所示:
①则反应速率υ(a)、υ(b)、υ(c)的大小关系是υ(a)>υ(b)=υ(c);
②下列可说明反应到达图中c点的是BC;
A.NO、CO、CO2、N2的浓度比值保持2:2:2:1不变
B.CO的浓度不再改变
C.反应消耗2molNO的同时消耗1molN2
D.容器中的气体质量或物质的量保持不变
(3)为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
【资料查阅】
A.不同的催化剂对同一反应的催化效率不同;
B.使用等质量相同的催化剂时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
| 实验编号 | 实验目的 | T/℃ | NO初始浓度 mol/L | CO初始浓度 mol/L | 同种催化剂的比表面积 m2/g | 达平衡时所用的时间min |
| Ⅰ | 参照实验 | 280 | 6.50×10-3 | 4.00×10-3 | 80 | t |
| Ⅱ | 280 | 6.50×10-3 | 4.00×10-3 | 120 | 0.5t | |
| Ⅲ | 360 | 6.50×10-3 | 4.00×10-3 | 80 | 0.2t |
②课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是温度,且升高温度反应速率将增大.(填“增大”、“减小”、“无影响”).
17.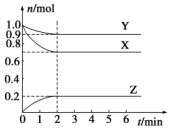 某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
(1)该反应的化学方程式为3X+Y?2Z.
(2)反应开始至2min,气体Z的反应速率为0.05mol•L-1•min-1.
(3)若X、Y、Z均为气体,反应达到平衡时,压强是开始时的0.90倍;此时放出了a kJ的热量,则按(1)的反应方程式写成热化学反应方程式时,该反应的反应热△H=-10akJ•mol-1.
(4)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.已知:
工业上通过氢气在氯气中充分燃烧制取HCl气体,写出该反应的热化学反应方程式:H2(g)+Cl2(g)=2HCl(g)△H=-184kJ•mol-1.
 某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:(1)该反应的化学方程式为3X+Y?2Z.
(2)反应开始至2min,气体Z的反应速率为0.05mol•L-1•min-1.
(3)若X、Y、Z均为气体,反应达到平衡时,压强是开始时的0.90倍;此时放出了a kJ的热量,则按(1)的反应方程式写成热化学反应方程式时,该反应的反应热△H=-10akJ•mol-1.
(4)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.已知:
| 化学键 | H-H | H-Cl | Cl-Cl |
| 键能/KJ•mol-1 | 436 | 431 | 242 |
16.实现下列变化时,需克服相同类型作用力的是( )
| A. | 水晶和干冰的熔化 | B. | 食盐和碘的熔化 | ||
| C. | 金刚石和白磷的熔化 | D. | 纯碱和烧碱的熔化 |
15.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | C. | 镁与稀硫酸反应 | D. | 氧化钙溶于水 |
14.常温下,用铁片和稀硫酸反应制氢气时,下列措施不能使氢气生成速率加快的是( )
| A. | 水浴加热 | B. | 将稀硫酸改为98%的浓硫酸 | ||
| C. | 滴加少许CuSO4溶液 | D. | 改用铁粉并振荡 |
13.根据热化学方程式:S(g)+O2(g)═SO2(g)△H=-Q KJ•mol-1,下列分析正确的是( )
| A. | 该反应的反应物总能量比产物总能量低QkJ | |
| B. | 1mol S(g)与1 mol O2(g)反应,生成1 mol SO2(g),放出Q kJ的热量 | |
| C. | 在S(s)+O2(g)═SO2(g) 反应中,生成1 mol SO2(g)放出的热量大于Q KJ | |
| D. | 1个S(g)与1个O2(g) 完全反应可以放出Q KJ的热量 |
12.含有元素硒(Se)的保健品已开始进入市场.已知它与氧同族,与钾同周期.则下列关于硒的叙述中,正确的是( )
| A. | 金属性比钾强 | B. | 最高价氧化物的化学式是SeO3 | ||
| C. | 高价含氧酸的酸性:H2SeO4>H2SO4 | D. | 氢化物稳定性:H2Se>H2O |
11.下列关于元素周期表的叙述中正确的是( )
0 162587 162595 162601 162605 162611 162613 162617 162623 162625 162631 162637 162641 162643 162647 162653 162655 162661 162665 162667 162671 162673 162677 162679 162681 162682 162683 162685 162686 162687 162689 162691 162695 162697 162701 162703 162707 162713 162715 162721 162725 162727 162731 162737 162743 162745 162751 162755 162757 162763 162767 162773 162781 203614
| A. | 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 | |
| B. | 元素周期表共七个横行代表七个周期,18 个纵横代表18 个族 | |
| C. | 主、副族元素的族序数从左到右都是依次由小到大排列(如ⅠB→→ⅦB) | |
| D. | 除零族外,由长、短周期元素共同组成的元素族称为主族 |