题目内容
15.下列反应中生成物总能量高于反应物总能量的是( )| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | C. | 镁与稀硫酸反应 | D. | 氧化钙溶于水 |
分析 反应中生成物总能量高于反应物总能量的是吸热反应,而常见的吸热反应有:绝大多数的分解反应;铵盐和碱的反应;以C、氢气或CO为还原剂的氧化还原反应等,以此解答该题.
解答 解:生成物总能量高于反应物总能量,为吸热反应,
A.碳酸钙受热分解,属于吸热反应,故A正确;
B.乙醇燃烧放出大量的热,属于放热反应,故B错误;
C.镁与稀硫酸反应,为活泼金属与酸的反应,属于放热反应,故C错误;
D.氧化钙与水反应生成氢氧化钙,属于放热反应,故D错误.
故选A.
点评 本题考查化学反应与能量变化,为高频考点,侧重考查学生的分析能力和双基的掌握,有利于培养学生良好的科学素养,难度不大,注意常见吸热反应与放热反应的类型.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
5.下列化学用语表示正确的是( )
| A. | 氯化钠的电子式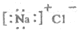 | B. | 次氯酸的电子式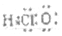 | ||
| C. | HCl分子的电子式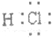 | D. | 氯原子的结构示意图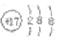 |
6.甲、乙是周期表中同一周期的两种元素,甲在ⅡA族,乙在ⅣA族,那么甲、乙两元素的原子序数之差不可能是( )
| A. | 2 | B. | 12 | C. | 26 | D. | 11 |
3.下列粒子属于等电子体的是( )
| A. | CO和N2 | B. | CH4和NH4+ | C. | NH2-和H2O2 | D. | HCl和H2O |
20.下列说法正确的是( )
| A. | SiO2不能与HNO3、H2SO4等所有的酸反应 | |
| B. | 由Na2CO3+SiO$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑可知硅酸的酸性比碳酸的酸性强 | |
| C. | 硅胶常用于做干燥剂 | |
| D. | CO2与SiO2均是酸性氧化物,溶于水均得到相应的酸 |
7.一定条件下,向2L恒容密闭容器中充入1mol PCl5,发生反应:PCl5(g)?PCl3(g)+Cl2(g)
反应过程中测定的部分数据见表(反应过程中条件不变):
请回答下列问题:
(1)x 的值是0.2;
(2)0-50s 内,用PCl3的浓度变化表示的化学反应速率是0.0016mol/(L•s);
(3)250s 以后,Cl2的物质的量不再改变的原因是250s达到平衡,正逆反应速率相等,条件不变,各组分的物质的量都不再变化;
(4)250s 时,容器中Cl2的物质的量是0.2mol,PCl5的物质的量是0.8mol,PCl5的转化率是20%.
反应过程中测定的部分数据见表(反应过程中条件不变):
| t/s | 0 | 30 | 150 | 250 | 350 | 450 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 | x |
(1)x 的值是0.2;
(2)0-50s 内,用PCl3的浓度变化表示的化学反应速率是0.0016mol/(L•s);
(3)250s 以后,Cl2的物质的量不再改变的原因是250s达到平衡,正逆反应速率相等,条件不变,各组分的物质的量都不再变化;
(4)250s 时,容器中Cl2的物质的量是0.2mol,PCl5的物质的量是0.8mol,PCl5的转化率是20%.
19.可以在实验室安全快速制取氨气的方法是( )
| A. | 在浓氨水中加固体NaOH | B. | 混合NH4Cl溶液和NaOH溶液 | ||
| C. | 加热分解NH4Cl晶体 | D. | 加热消石灰和NH4NO3的固体混合物 |