11.下列化合物中,既存在离子键又存在共价键的是( )
| A. | 硫酸钠 | B. | 乙酸 | C. | 氯化镁 | D. | 二氧化碳 |
10.下列有关物质的性质与应用对应的是( )
| A. | NH4Cl受热易分解,可用于实验室制氨气 | |
| B. | 液氨汽化时能吸收大量的热,使周围温度急剧降低,因此可用作制冷剂 | |
| C. | NO2气体有毒,且可以和水反应,实验室多余的NO2气体用水吸收即可 | |
| D. | N2性质稳定,工业生产金属镁时,为防止其氧化,可以用N2作保护气 |
8.下列各装置能够达到相应实验目的是( )
| A. | 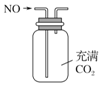 用图所示装置(正放)可收集NO气体 | |
| B. | 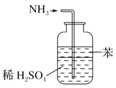 用图所示装置可吸收多余氨气且能防止倒吸 | |
| C. | 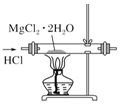 用装置制取无水MgCl2 | |
| D. | 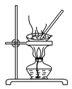 用装置蒸干NH4Cl饱和溶液获取NH4Cl晶体 |
7.在含有大量Ba2+、H+、NO${\;}_{3}^{-}$的溶液中,还可能大量共存的离子是( )
| A. | Fe2+ | B. | NH${\;}_{4}^{+}$ | C. | HCO${\;}_{3}^{-}$ | D. | OH- |
4.实验室用卤块(主要成分为MgCl2•6H2O,含有MgSO4.FeCl2等杂质)制备少量Mg(ClO3)2•6H2O的流程如图1:
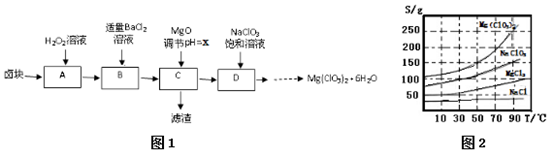
已知:①四种化合物的溶解度(S)随温度(T)变化曲线如图2所示.
②室温时一些物质的Ksp如表:
③Mg(ClO3)2有较强的氧化性,其还原产物是Cl-.
(1)H2O2的电子式为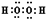
(2)滤渣的成分是Fe(OH)3、BaSO4(填化学式);
(3)经测定,D中铁离子的浓度为1×10-5 mol/L,则x为3.3
(4)D中所发生的化学反应方程式式为MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,框图中由D→…→制Mg(ClO3)2•6H2O晶体的实验步骤依次为:①加热蒸发;②趁热过滤(请补充);③冷却结晶;④过滤洗涤.
(5)产品中Mg(ClO3)2•6H2O含量的测定:
步骤1:准确称量3.50g产品配成100mL溶液.
步骤2:取10.00mL试液于锥形瓶中,加入10.00mL稀硫酸和20.00mL 1.000mol/L的FeSO4溶液,微热.
步骤3:冷却至室温,用0.100mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点.
步骤4:将步骤2、3重复两次
①步骤3中发生反应的离子方程式Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
②步骤3中若滴定前不用标准液润洗滴定管,将会导致最终结果偏小(填“偏大”.“偏小”或“不变”).
③若平均消耗K2Cr2O7溶液15.00mL,则产品中Mg(ClO3)2•6H2O(其M=299g/mol)的质量分数为78.3%.

已知:①四种化合物的溶解度(S)随温度(T)变化曲线如图2所示.
②室温时一些物质的Ksp如表:
| 化学式 | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 8.0×10-38 | 1.8x10-11 |
(1)H2O2的电子式为
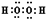
(2)滤渣的成分是Fe(OH)3、BaSO4(填化学式);
(3)经测定,D中铁离子的浓度为1×10-5 mol/L,则x为3.3
(4)D中所发生的化学反应方程式式为MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,框图中由D→…→制Mg(ClO3)2•6H2O晶体的实验步骤依次为:①加热蒸发;②趁热过滤(请补充);③冷却结晶;④过滤洗涤.
(5)产品中Mg(ClO3)2•6H2O含量的测定:
步骤1:准确称量3.50g产品配成100mL溶液.
步骤2:取10.00mL试液于锥形瓶中,加入10.00mL稀硫酸和20.00mL 1.000mol/L的FeSO4溶液,微热.
步骤3:冷却至室温,用0.100mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点.
步骤4:将步骤2、3重复两次
①步骤3中发生反应的离子方程式Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
②步骤3中若滴定前不用标准液润洗滴定管,将会导致最终结果偏小(填“偏大”.“偏小”或“不变”).
③若平均消耗K2Cr2O7溶液15.00mL,则产品中Mg(ClO3)2•6H2O(其M=299g/mol)的质量分数为78.3%.
2.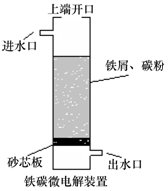 铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如图.若上端开口关闭,可得到强还原性的H•(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的•OH(羟基自由基).下列说法正确的是( )
铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如图.若上端开口关闭,可得到强还原性的H•(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的•OH(羟基自由基).下列说法正确的是( )
0 162564 162572 162578 162582 162588 162590 162594 162600 162602 162608 162614 162618 162620 162624 162630 162632 162638 162642 162644 162648 162650 162654 162656 162658 162659 162660 162662 162663 162664 162666 162668 162672 162674 162678 162680 162684 162690 162692 162698 162702 162704 162708 162714 162720 162722 162728 162732 162734 162740 162744 162750 162758 203614
 铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如图.若上端开口关闭,可得到强还原性的H•(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的•OH(羟基自由基).下列说法正确的是( )
铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如图.若上端开口关闭,可得到强还原性的H•(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的•OH(羟基自由基).下列说法正确的是( )| A. | 无论是否鼓入空气,负极的电极反应式均为Fe-3e-=Fe3+ | |
| B. | 鼓入空气时,每生成1mol•OH有2mol电子发生转移 | |
| C. | 不鼓入空气时,正极的电极反应式为H++e-=H• | |
| D. | 处理含有C2O42-的污水时,上端开口应关闭 |
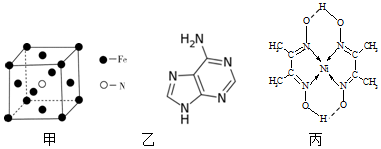
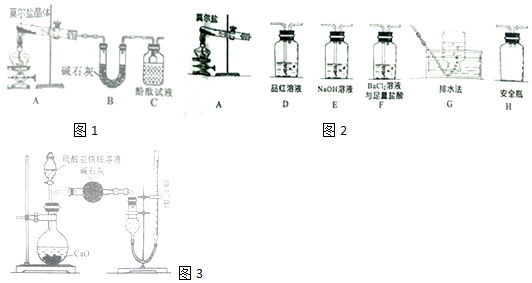

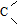 →-N=
→-N=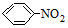 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$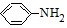 (易被氧化).请回答:
(易被氧化).请回答: ;
;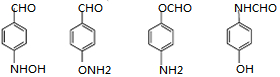 ;
;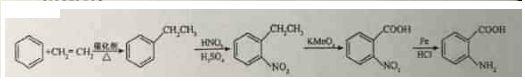 .
.