3.已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
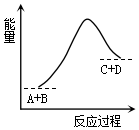

| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 该反应只有在加热条件下才能进行 | |
| C. | 该反应为放热反应 | |
| D. | 该反应为吸热反应 |
2.下列物质的沸点变化顺序正确的是( )
| A. | CH4>SiH4>GeH4>SnH4 | B. | NH3<PH3<AsH3<SbH3 | ||
| C. | H2O>H2S>H2Se>H2Te | D. | HCl<HBr<HI<HF |
1.根据表中信息,下列叙述正确的是( )
| 短周期元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的热稳定性:H2T<H2R | |
| B. | 单质与稀盐酸反应的速率:L<Q | |
| C. | 离子半径:R2-<L2+ | |
| D. | M与T形成的化合物既能与强酸反应,又能与强碱反应 |
20.下列各原子或离子的电子排布式错误的是( )
| A. | K+ 1s22s22p63s23p6 | B. | F 1s22s22p5 | ||
| C. | S2- 1s22s22p63s23p4 | D. | Ar 1s22s22p63s23p6 |
18.短周期主族元素X、Y、Z、W的原子序数依次增大.X与W同主族,X、W的单质在标准状况下的状态不同.Y是空气中含量最高的元素,Z原子最外层电子数是其内层电子总数的3倍,Z2-与W+有相同的电子层结构.下列说法正确的是( )
| A. | 原子半径大小:r(W)>r(Z)>r(Y)>r(X) | |
| B. | 元素Y的简单气态氢化物的热稳定性和熔沸点都比Z的高 | |
| C. | 化合物X2Z2与 W2Z2所含化学键类型完全相同 | |
| D. | 只含X、Y、Z三种元素组成物质的水溶液可能呈酸性或碱性 |
17.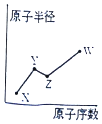 X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( )
 X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( )| A. | Y、Z、W处于同一周期 | |
| B. | X、Y、Z、W的原子序数递增 | |
| C. | X、W可形成化学式为XW的离子化合物 | |
| D. | 简单离子半径是Z大于W |
15.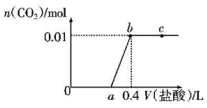 向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )
向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )
0 162488 162496 162502 162506 162512 162514 162518 162524 162526 162532 162538 162542 162544 162548 162554 162556 162562 162566 162568 162572 162574 162578 162580 162582 162583 162584 162586 162587 162588 162590 162592 162596 162598 162602 162604 162608 162614 162616 162622 162626 162628 162632 162638 162644 162646 162652 162656 162658 162664 162668 162674 162682 203614
 向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )
向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )| A. | a点时溶液中存在c(Na+)=c(HCO3-)+C(CO32-)+c(H2CO3) | |
| B. | 0~a段溶液中水电离出的OH-浓度先增大后减小 | |
| C. | a=0.2 | |
| D. | ab段发生反应的离子方程式为CO32-+2H+═H2O+CO2↑ |
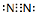 .下列能实现人工固氮的是D.
.下列能实现人工固氮的是D.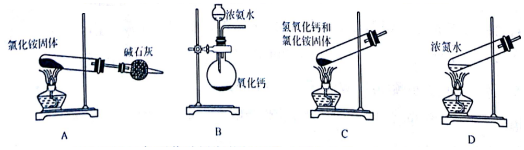
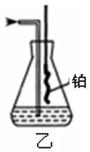
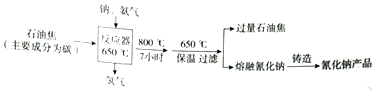

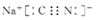 .
.