题目内容
14.分子式为C5H12O的醇,能被酸性KMnO4溶液氧化成C5H10O,则符合此条件的醇的同分异构体(不考虑立体异构)最多有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 3种 |
分析 先书写戊基-C5H11异构体,戊基异构数目等于戊醇的异构体数目,分子式为C5H12O的醇,能被酸性KMnO4溶液氧化成C5H10O,则与羟基所连碳上只含有1个氢原子,以此确定醇的结构简式.
解答 解:戊基-C5H11可能的结构有8种:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-CH(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,戊基异构数目等于戊醇的异构体数目,分子式为C5H12O的醇有8种结构,其中能被酸性KMnO4溶液氧化成C5H10O,则与羟基所连碳上只含有1个氢原子,符合此条件的醇的同分异构体(不考虑立体异构)最多有4种:HOCH(CH3)CH2CH2CH3、HOCH(CH2CH3)2、HOCHCH(CH3)CH2CH3、HOCH(CH3)CH(CH3)2,故选A.
点评 本题考查有机物的推断、同分异构体的书写等,难度中等,可以利用烃基异构判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列说法中正确的是( )
| A. | 1mol任何物质都含有6.02×1023个分子 | |
| B. | 在相同条件下,相同物质的量CO、N2的混合气体与O2的分子个数相同,原子个数也相同 | |
| C. | NaOH的摩尔质量40g | |
| D. | 在标准状况下,1molO2与1molSO3的体积相同 |
2.锂离子电池的应用很广,一种利用钛铁矿[主要成分为偏钛酸亚铁(FeTiO3),含有少量Fe2O3]制取钛白粉(TiO2)和利用其副产物制取锂离子电池的正极材料(LiFePO4)的工艺流程如图(部分条件未给出).
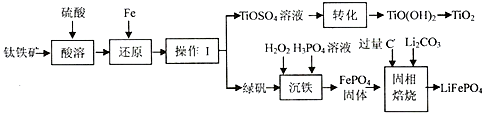
(1)FeTiO3中Ti的化合价为+4;在“还原”步骤中,还原“Fe3+”的反应中氧化剂和还原剂之比为2:1.
(2)FeSO4溶解度与温度关系如表,
则操作I 的名称为蒸发浓缩、冷却结晶、过滤.
(3)“转化”步骤中对溶液进行加热的主要目的是加快和促进水解.
(4)写出“沉铁”的离子反应方程式2Fe2++H2O2+2H3PO4=2FePO4↓+2H2O+4H+,为使Fe3+完全沉降,则PO43-的浓度至少应为9.91×10-11mol/L(己知:ksp (FePO4•2H2O)=9.91×10-16).
(5)流程中可循环利用的物质是(H2O除外)H2SO4,写出固相焙烧的反应方程式2FePO4+Li2CO3+2C$\frac{\underline{\;焙烧\;}}{\;}$2LiFePO4+3CO↑.
(6)某锂离子充放电时,正极发生LiFePO4与FePO4的转化,当充电时,电池负极发生的反应为6C+xLi++xe-=LixC6,写出放电时电池反应方程式xFePO4+LixC6=6C+xLiFePO4.

(1)FeTiO3中Ti的化合价为+4;在“还原”步骤中,还原“Fe3+”的反应中氧化剂和还原剂之比为2:1.
(2)FeSO4溶解度与温度关系如表,
| 温度(℃) | 30 | 20 | l5 | l0 | 5 | 0 | -2 | -6 |
| FeSO4(g/L) | 240 | 190 | 130 | 117 | 95 | 79 | 59 | 38 |
(3)“转化”步骤中对溶液进行加热的主要目的是加快和促进水解.
(4)写出“沉铁”的离子反应方程式2Fe2++H2O2+2H3PO4=2FePO4↓+2H2O+4H+,为使Fe3+完全沉降,则PO43-的浓度至少应为9.91×10-11mol/L(己知:ksp (FePO4•2H2O)=9.91×10-16).
(5)流程中可循环利用的物质是(H2O除外)H2SO4,写出固相焙烧的反应方程式2FePO4+Li2CO3+2C$\frac{\underline{\;焙烧\;}}{\;}$2LiFePO4+3CO↑.
(6)某锂离子充放电时,正极发生LiFePO4与FePO4的转化,当充电时,电池负极发生的反应为6C+xLi++xe-=LixC6,写出放电时电池反应方程式xFePO4+LixC6=6C+xLiFePO4.
9.分子式为 C7H16的烷烃中,含有三个甲基的同分异构体共几种( )
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4 种 |
6.下列有机实验操作或叙述正确的是( )
| A. | 将乙烯和乙炔气体分别通入溴的四氯化碳溶液中,两者都褪色 | |
| B. | 甲烷和氯气在室温下的光照环境中可以稳定存在 | |
| C. | 苯能使溴水褪色是因为二者反应生成了溴苯 | |
| D. | 要除去乙烷中的乙烯制得纯净的乙烷,将混合气体通入酸性高锰酸钾溶液中 |
3.金属镓是一种广泛用于电子工业和通讯领域的重要金属,镓元素(31Ga)在元素周期表中位于第四周期,ⅢA族,化学性质与铝元素相似.
(1)工业上利用Ga与NH3合成固体半导体材料氮化镓(GaN)同时有氢气生成,反应中,生成3mol H2时放出30.8KJ的热.
①反应的热化学方程式是2Ga(s)+2NH3(g)?2GaN(s)+3H2(g)△H=-30.8KJ/mol.
②反应的化学平衡常数表达式是$\frac{{c}^{3}({H}_{2})}{{c}^{2}(N{H}_{3})}$;温度升高时,反应的平衡常数变小.(填“变大”“变小”或“不变”)
③在密闭体系内进行上述可逆反应,下列有关表达正确的是A.

A.图象Ⅰ中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压
B.图象Ⅱ中纵坐标可以为镓的转化率
C.图象Ⅲ中纵坐标可以为化学反应速率
D.图象Ⅳ中纵坐标可以为体系内混合气体平均相对分子质量
④氮化镓(GaN)性质稳定,但能缓慢的溶解在热的NaOH溶液中,该反应的离子方程式是GaN+OH-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$GaO2-+NH3↑.
(2)将一块镓铝合金完全溶于烧碱溶液中得到溶液X.已知:
往X溶液中缓缓通入CO2,最先析出的氢氧化物是Al(OH)3.
(3)工业上电解精炼镓的原理如下:待提纯的粗镓(内含Zn、Fe、Cu杂质)为阳极,高纯度镓为阴极,NaOH溶液为电解质溶液.在电流作用下使粗镓在阳极溶解进入电解质溶液,离子迁移到达阴极并在阴极放出电析出高纯镓.
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+,电解精炼镓时阳极泥的成分是Fe、Cu.
②GaO2-在阴极放电的电极方程式是GaO2-+3e-+2H2O=Ga+4OH-.
(1)工业上利用Ga与NH3合成固体半导体材料氮化镓(GaN)同时有氢气生成,反应中,生成3mol H2时放出30.8KJ的热.
①反应的热化学方程式是2Ga(s)+2NH3(g)?2GaN(s)+3H2(g)△H=-30.8KJ/mol.
②反应的化学平衡常数表达式是$\frac{{c}^{3}({H}_{2})}{{c}^{2}(N{H}_{3})}$;温度升高时,反应的平衡常数变小.(填“变大”“变小”或“不变”)
③在密闭体系内进行上述可逆反应,下列有关表达正确的是A.

A.图象Ⅰ中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压
B.图象Ⅱ中纵坐标可以为镓的转化率
C.图象Ⅲ中纵坐标可以为化学反应速率
D.图象Ⅳ中纵坐标可以为体系内混合气体平均相对分子质量
④氮化镓(GaN)性质稳定,但能缓慢的溶解在热的NaOH溶液中,该反应的离子方程式是GaN+OH-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$GaO2-+NH3↑.
(2)将一块镓铝合金完全溶于烧碱溶液中得到溶液X.已知:
| Al(OH)3 | Ga(OH)3 | |
| 酸式电离常数Ka | 2×10-11 | 1×10-2 |
| 碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
(3)工业上电解精炼镓的原理如下:待提纯的粗镓(内含Zn、Fe、Cu杂质)为阳极,高纯度镓为阴极,NaOH溶液为电解质溶液.在电流作用下使粗镓在阳极溶解进入电解质溶液,离子迁移到达阴极并在阴极放出电析出高纯镓.
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+,电解精炼镓时阳极泥的成分是Fe、Cu.
②GaO2-在阴极放电的电极方程式是GaO2-+3e-+2H2O=Ga+4OH-.
3.如图所示,φ(X)为气态反应物在平衡混合物中的体积分数,T为温度.符合该曲线的反应是( )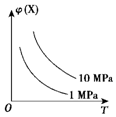

| A. | N2(g)+3H2(g)?2NH3(g)△H<0 | B. | 2HI(g)?H2(g)+I2(g)△H>0 | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 | D. | C(s)+H2O(g)?H2(g)+CO(g)△H>0 |
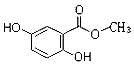
 .
.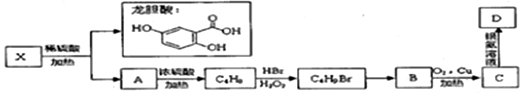
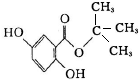 ,C4H9Br→B的化学反应是取代反应.
,C4H9Br→B的化学反应是取代反应. .
.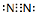 .下列能实现人工固氮的是D.
.下列能实现人工固氮的是D.