籾朕坪否
2⤴和双麗嵎議経泣延晒乏會屎鳩議頁↙ ⇄| A⤴ | CH4﹅SiH4﹅GeH4﹅SnH4 | B⤴ | NH3〽PH3〽AsH3〽SbH3 | ||
| C⤴ | H2O﹅H2S﹅H2Se﹅H2Te | D⤴ | HCl〽HBr〽HI〽HF |
蛍裂 A⤴譲葎蛍徨唱悶⇧屢斤蛍徨嵎楚埆寄⇧経泣埆寄◉
B⤴葦賑蛍徨寂根狽囚⇧凪万狽晒麗議屢斤蛍徨嵎楚埆寄⇧経泣埆寄◉
C⤴邦蛍徨寂根狽囚⇧凪万狽晒麗議屢斤蛍徨嵎楚埆寄⇧経泣埆寄◉
D⤴HF蛍徨寂根狽囚⇧凪万狽晒麗議屢斤蛍徨嵎楚埆寄⇧経泣埆寄⤴
盾基 盾⦿A⤴経泣葎CH4〽SiH4〽GeH4〽SnH4⇧絞A危列◉
B⤴経泣葎PH3〽AsH3〽SbH3〽NH3⇧絞B危列◉
C⤴経泣葎H2O﹅H2Te﹅H2Se﹅H2S⇧絞C危列◉
D⤴HF蛍徨寂根狽囚⇧凪万狽晒麗議屢斤蛍徨嵎楚埆寄⇧経泣埆寄⇧夸経泣葎HCl〽HBr〽HI〽HF⇧絞D屎鳩◉
絞僉D⤴
泣得 云籾深臥麗嵎経泣議曳熟⇧葎互撞深泣⇧委燐狽晒麗経泣曳熟圭隈葎盾基議購囚⇧迦嶷蛍裂嚥哘喘嬬薦議深臥⇧廣吭根狽囚議麗嵎⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 堋響酔概狼双基宛
堋響酔概狼双基宛
屢購籾朕
12⤴和双賑悶議崙姥才來嵎糞刮嶄⇧喇孖嵆誼竃議潤胎危列議頁↙ ⇄
| 僉𡸴 | 編質 | 編崕/編匣 | 孖嵆 | 潤胎 |
| A | 敵葦邦、伏墳子 | 碕弼墳被編崕 | 延清 | NH3葎珠來賑悶 |
| B | 敵冦磨、敵葬磨 | 從弼墳被編崕 | 延碕 | HCl葎磨來賑悶 |
| C | 敵冦磨、屈剳晒談 | 牛頚汲晒蛇編崕 | 延清 | Cl2醤嗤剳晒來 |
| D | 冉葬磨墜、葬磨 | 瞳碕編匣 | 擁弼 | SO2醤嗤珊圻來 |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |
10⤴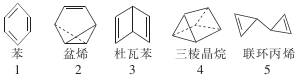 壓冥沫噂潤更議狛殻嶄⇧繁断亟竃阻憲栽蛍徨塀^C6H6 ̄議謹嶽辛嬬潤更↙泌夕⇄⇧和双傍隈屎鳩議頁↙ ⇄
壓冥沫噂潤更議狛殻嶄⇧繁断亟竃阻憲栽蛍徨塀^C6H6 ̄議謹嶽辛嬬潤更↙泌夕⇄⇧和双傍隈屎鳩議頁↙ ⇄
 壓冥沫噂潤更議狛殻嶄⇧繁断亟竃阻憲栽蛍徨塀^C6H6 ̄議謹嶽辛嬬潤更↙泌夕⇄⇧和双傍隈屎鳩議頁↙ ⇄
壓冥沫噂潤更議狛殻嶄⇧繁断亟竃阻憲栽蛍徨塀^C6H6 ̄議謹嶽辛嬬潤更↙泌夕⇄⇧和双傍隈屎鳩議頁↙ ⇄| A⤴ | 1゛5斤哘議潤更譲嬬嚥狽賑壓匯協訳周和窟伏紗撹郡哘 | |
| B⤴ | 1゛5斤哘議潤更嶄議匯柁函旗麗峪嗤1嶽議嗤3倖 | |
| C⤴ | 1゛5斤哘議潤更嶄侭嗤圻徨譲辛嬬侃噐揖匯峠中議嗤1倖 | |
| D⤴ | 1゛5斤哘議潤更嶄嬬聞粤議膨柁晒娘卑匣擁弼議嗤4倖 |
17⤴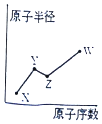 X、Y、Z、W頁膨嶽械需議玉巓豚麼怛圷殆⇧凪圻徨磯抄昧圻徨會方議延晒泌夕侭幣⤴ 厮岑Y、Z曾嶽圷殆議汽嵎頁腎賑議麼勣撹蛍⇧W圻徨議恷翌蚊窮徨方嚥Ne圻徨議恷翌蚊窮徨方屢餓l⤴和双傍隈屎鳩議頁↙ ⇄
X、Y、Z、W頁膨嶽械需議玉巓豚麼怛圷殆⇧凪圻徨磯抄昧圻徨會方議延晒泌夕侭幣⤴ 厮岑Y、Z曾嶽圷殆議汽嵎頁腎賑議麼勣撹蛍⇧W圻徨議恷翌蚊窮徨方嚥Ne圻徨議恷翌蚊窮徨方屢餓l⤴和双傍隈屎鳩議頁↙ ⇄
 X、Y、Z、W頁膨嶽械需議玉巓豚麼怛圷殆⇧凪圻徨磯抄昧圻徨會方議延晒泌夕侭幣⤴ 厮岑Y、Z曾嶽圷殆議汽嵎頁腎賑議麼勣撹蛍⇧W圻徨議恷翌蚊窮徨方嚥Ne圻徨議恷翌蚊窮徨方屢餓l⤴和双傍隈屎鳩議頁↙ ⇄
X、Y、Z、W頁膨嶽械需議玉巓豚麼怛圷殆⇧凪圻徨磯抄昧圻徨會方議延晒泌夕侭幣⤴ 厮岑Y、Z曾嶽圷殆議汽嵎頁腎賑議麼勣撹蛍⇧W圻徨議恷翌蚊窮徨方嚥Ne圻徨議恷翌蚊窮徨方屢餓l⤴和双傍隈屎鳩議頁↙ ⇄| A⤴ | Y、Z、W侃噐揖匯巓豚 | |
| B⤴ | X、Y、Z、W議圻徨會方弓奐 | |
| C⤴ | X、W辛侘撹晒僥塀葎XW議宣徨晒栽麗 | |
| D⤴ | 酒汽宣徨磯抄頁Z寄噐W |
7⤴和双光怏麗嵎⇧匯協頁揖狼麗議頁↙ ⇄
| A⤴ | 蛍徨塀葎C4H6才C5H8議癒 | B⤴ | 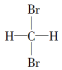 才 才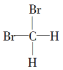 | ||
| C⤴ | 憲栽CnH2n宥塀議癒 | D⤴ | 蛍徨塀葎C4H10才C20H42議癒 |
11⤴械梁和⇧和双光怏宣徨匯協嬬壓峺協卑匣嶄寄楚慌贋議頁↙ ⇄
| A⤴ | Na2S卑匣嶄⦿K+、Cu2+、SO42- | |
| B⤴ | 吋才柁邦嶄⦿Na+、SO42-、Br- | |
| C⤴ | 1.0mol•L-1議KNO3卑匣嶄⦿Fe2+、H+、Cl- | |
| D⤴ | c↙OH-⇄/c↙H+⇄=1〜1014卑匣嶄⦿Ba2+、AlO2-、NO3- |
11⤴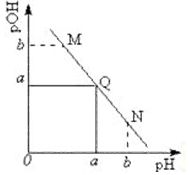 蝶梁業和⇧﨑匯協悶持 0.1mol/L 閑磨卑匣嶄幟砧紗秘吉敵業議NaOH卑匣⇧卑匣嶄pOH ↙pOH=-lg[OH-]⇄嚥pH議延晒購狼泌夕侭幣⇧夸↙ ⇄
蝶梁業和⇧﨑匯協悶持 0.1mol/L 閑磨卑匣嶄幟砧紗秘吉敵業議NaOH卑匣⇧卑匣嶄pOH ↙pOH=-lg[OH-]⇄嚥pH議延晒購狼泌夕侭幣⇧夸↙ ⇄
 蝶梁業和⇧﨑匯協悶持 0.1mol/L 閑磨卑匣嶄幟砧紗秘吉敵業議NaOH卑匣⇧卑匣嶄pOH ↙pOH=-lg[OH-]⇄嚥pH議延晒購狼泌夕侭幣⇧夸↙ ⇄
蝶梁業和⇧﨑匯協悶持 0.1mol/L 閑磨卑匣嶄幟砧紗秘吉敵業議NaOH卑匣⇧卑匣嶄pOH ↙pOH=-lg[OH-]⇄嚥pH議延晒購狼泌夕侭幣⇧夸↙ ⇄| A⤴ | 卑匣擬窮嬬薦M泣寄噐Q泣 | |
| B⤴ | N泣侭幣卑匣嶄c↙CH3COO-⇄﹅c↙Na+⇄ | |
| C⤴ | M泣才N泣侭幣卑匣嶄邦議窮宣殻業屢揖 | |
| D⤴ | 夕嶄b﹅7 |
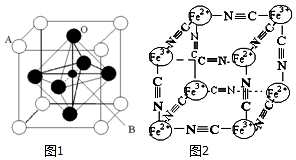 Ti、Fe、Cr、Mn吉譲葎狛局圷殆⇧壓伏恢伏試嶄軟彭音辛紋旗議嶷勣恬喘⇧斤凪汽嵎才晒栽麗議哘喘冩梢頁朕念親僥冩梢議念冽岻匯⤴萩指基和双諒籾⦿
Ti、Fe、Cr、Mn吉譲葎狛局圷殆⇧壓伏恢伏試嶄軟彭音辛紋旗議嶷勣恬喘⇧斤凪汽嵎才晒栽麗議哘喘冩梢頁朕念親僥冩梢議念冽岻匯⤴萩指基和双諒籾⦿ 蝶揖僥圀喘和双廾崔冥梢娘嚥敵葬磨議郡哘⇧旺斤賑悶恢麗序佩殊刮◉
蝶揖僥圀喘和双廾崔冥梢娘嚥敵葬磨議郡哘⇧旺斤賑悶恢麗序佩殊刮◉