18.下列反应可用离子方程式“H++OH-→H2O”表示的是( )
| A. | H2SO4溶液与Ba(OH)2溶液混合 | B. | NH3•H2O溶液与HCl溶液混合 | ||
| C. | NaHCO3溶液与NaOH溶液混合 | D. | HNO3溶液与KOH溶液混合 |
17.下列化学用语正确的是( )
| A. | N原子的轨道表示式: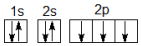 | B. | 氧化钠的分子式:Na2O | ||
| C. | 碳-14原子表示为:14C | D. | Na2S的电子式: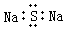 |
16.含有非极性共价键的离子化合物是( )
| A. | HC≡CH | B. | KOH | C. | Na2O2 | D. | CaCl2 |
15.对稳定人体血液的pH起重要作用的离子是( )
| A. | Na+ | B. | HCO3- | C. | Fe2+ | D. | Cl- |
14.在常温常压下,将100mLH2S与O2混合气体在一定条件下充分反应后,恢复到原来的状况,剩余气体25mL.下列判断错误的是( )
| A. | 原混合气体中H2S的体积可能是75mL | |
| B. | 原混合气体中O2的体积可能是50mL | |
| C. | 剩余25 mL气体可能全部是SO2 | |
| D. | 剩余25 mL气体可能是SO2与O2 |
13.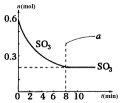 在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2(g)+O2(g)-Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是( )
在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2(g)+O2(g)-Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是( )
 在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2(g)+O2(g)-Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是( )
在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2(g)+O2(g)-Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是( )| A. | 0~8min内v(SO3)=0.025mol/(L•min) | |
| B. | 8min时,v逆(SO2)=2v正 (O2) | |
| C. | 8min时,容器内压强保持不变 | |
| D. | 若8min时将容器压缩为1L,n(SO3)的变化如图中a |
12.某温度下,一反应平衡常数K=$\frac{{c}_{CO}×{c}_{{H}_{2}O}}{{c}_{C{O}_{2}}×{c}_{{H}_{2}}}$.恒容时到达平衡后,升高温度,H2浓度减小.下列说法正确的是( )
| A. | 升温,逆反应速率减小 | B. | 加压,H2浓度减小 | ||
| C. | 增加H2,K减小 | D. | 该反应的正反应是吸热反应 |
11.5.5g铁铝混合物与足量的盐酸反应,生成标准状况下的氢气4.48L,则混合物中Fe与Al的物质的量之比( )
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 2:3 |
10. 反应 2X(g)+3Y(g)?Z(g)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间的关系如图所示.若使曲线a变为曲线b,可采取( )
反应 2X(g)+3Y(g)?Z(g)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间的关系如图所示.若使曲线a变为曲线b,可采取( )
 反应 2X(g)+3Y(g)?Z(g)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间的关系如图所示.若使曲线a变为曲线b,可采取( )
反应 2X(g)+3Y(g)?Z(g)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间的关系如图所示.若使曲线a变为曲线b,可采取( )| A. | 降低温度 | B. | 减小压强 | C. | 加入催化剂 | D. | 增大Y的浓度 |
9.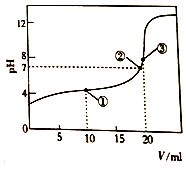 298K时,向20.00mL0.1mol/LHR溶液中滴加等浓度的NaOH 溶液,反应后溶液的pH与滴加的NaOH 溶液体积(V)的关系如图所示.下列说法正确的是( )
298K时,向20.00mL0.1mol/LHR溶液中滴加等浓度的NaOH 溶液,反应后溶液的pH与滴加的NaOH 溶液体积(V)的关系如图所示.下列说法正确的是( )
0 162449 162457 162463 162467 162473 162475 162479 162485 162487 162493 162499 162503 162505 162509 162515 162517 162523 162527 162529 162533 162535 162539 162541 162543 162544 162545 162547 162548 162549 162551 162553 162557 162559 162563 162565 162569 162575 162577 162583 162587 162589 162593 162599 162605 162607 162613 162617 162619 162625 162629 162635 162643 203614
 298K时,向20.00mL0.1mol/LHR溶液中滴加等浓度的NaOH 溶液,反应后溶液的pH与滴加的NaOH 溶液体积(V)的关系如图所示.下列说法正确的是( )
298K时,向20.00mL0.1mol/LHR溶液中滴加等浓度的NaOH 溶液,反应后溶液的pH与滴加的NaOH 溶液体积(V)的关系如图所示.下列说法正确的是( )| A. | HR溶液中只含有一种分子和三种离子 | |
| B. | 在①②③点对于的溶液中,②点水的电离程度最大 | |
| C. | ③点对应的溶液中有c(R-)>c(Na+)>c(H+)>c(OH-) | |
| D. | ①点对应的溶液中R-的水解程度小于HR的电离程度 |