18.亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强.
(I)经查:①Ksp(AgNO2)=2.0×10-8,Ksp(AgCl)=1.8×10-10;③Ka(HNO2)=5.1×10-4.请设计最简单的方法鉴别NaNO2和NaCl两种固体分别取两种固体样品少量于试管中加水溶解,再分别滴加酚酞试液,变红色的为NaNO2.
(Ⅱ)某化学实验小组用如图装置(略去夹持仪器)制备亚硝酸钠,并测定其产品的质量分数.
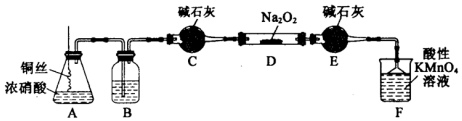
已知:①2NO+Na2O2═2NaNO2;
②酸性条件下,NO和NO2均能与MnO4-反应生成NO3-和Mn2+.
(1)这样使用铜丝的优点是可以控制反应的发生与停止.
(2)装置A中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;装置B中盛放的药品是C(填序号).
①浓硫酸②NaOH溶液③水④四氯化碳
(3)该小组取5.000g制取的样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.100mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如表:
①第一次实验数据出现异常,造成这种异常的原因可能是bc(填代号).
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O.
③该样品中亚硝酸钠的质量分数为69.0%.
(I)经查:①Ksp(AgNO2)=2.0×10-8,Ksp(AgCl)=1.8×10-10;③Ka(HNO2)=5.1×10-4.请设计最简单的方法鉴别NaNO2和NaCl两种固体分别取两种固体样品少量于试管中加水溶解,再分别滴加酚酞试液,变红色的为NaNO2.
(Ⅱ)某化学实验小组用如图装置(略去夹持仪器)制备亚硝酸钠,并测定其产品的质量分数.

已知:①2NO+Na2O2═2NaNO2;
②酸性条件下,NO和NO2均能与MnO4-反应生成NO3-和Mn2+.
(1)这样使用铜丝的优点是可以控制反应的发生与停止.
(2)装置A中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;装置B中盛放的药品是C(填序号).
①浓硫酸②NaOH溶液③水④四氯化碳
(3)该小组取5.000g制取的样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.100mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如表:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMn04溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O.
③该样品中亚硝酸钠的质量分数为69.0%.
17.将一定量的由Cu和Cu2O组成的混合粉末加入到125mL2.6mol•L-1的硝酸中,固体恰好完全溶解,得蓝色溶液X并收集到VmL(标准状况)的纯净无色气体Y.下列结论正确的是( )
| A. | X中有两种溶质 | |
| B. | Y通入纯水中得到酸性溶液 | |
| C. | 原混合粉末的总质量小于7.8g | |
| D. | 当V=1680时,原混合粉末中Cu和Cu2O的物质的量之比为8:1 |
16.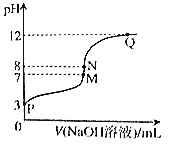 T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )
T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )
 T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )
T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )| A. | T℃时,CH3COOH电离平衡常数Ka=1.0×10-3 | |
| B. | M点对应的NaOH溶液体积为20.00mL | |
| C. | N点与Q点所示溶液中水的电离程度:N>Q | |
| D. | N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
14.莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是( )
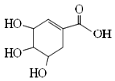

| A. | 分子式为C7H6O5 | B. | 分子中含有两种官能团 | ||
| C. | 1mol该有机物能与4molNaOH反应 | D. | 可发生加成和取代反应 |
13.下列各组中的两个反应所属反应类型相同的是( )
| A. | 光照甲烷和氯气的混合气体,混合气体颜色变浅;乙烯能使溴水褪色 | |
| B. | 乙烷在氧气中燃烧;乙烯在氧气中燃烧 | |
| C. | 乙烯能使溴水褪色;乙烯能使酸性高锰酸钾溶液褪色 | |
| D. | 工业上由乙烯和水反应生成乙醇;乙烯能使酸性高锰酸钾溶液褪色 |
12.在H2SO4、K2SO4、Al2(SO4)3和明矾的混合溶液中,H+的浓度为0.2mol/L,SO42-的浓度为0.5mol/L,当加入等体积0.6mol/L KOH溶液时,生成的沉淀恰好完全溶解.则反应后溶液中K+的浓度约为( )
| A. | 0.225mol/L | B. | 0.25mol/L | C. | 0.45mol/L | D. | 0.55mol/L |
11.已知R元素的某种同位素能形成化合物AmRn,其中A的化合价为+n.该化合物中一个R微粒的核外电子数为a,核内中子数为b,则该同位素的原子符号是( )
| A. | ${\;}_{a+m}^{b+m+n}R$ | B. | ${\;}_{a+m}^{b+a-m}R$ | C. | ${\;}_{a}^{b+a}R$ | D. | ${\;}_{a-m}^{a-m+b}R$ |
10.常见的有机反应类型有( ):
①取代 ②加成 ③消去 ④酯化 ⑤加聚 ⑥水解 ⑦还原.其中能在有机化合物中引入-OH的反应类型有.
0 162426 162434 162440 162444 162450 162452 162456 162462 162464 162470 162476 162480 162482 162486 162492 162494 162500 162504 162506 162510 162512 162516 162518 162520 162521 162522 162524 162525 162526 162528 162530 162534 162536 162540 162542 162546 162552 162554 162560 162564 162566 162570 162576 162582 162584 162590 162594 162596 162602 162606 162612 162620 203614
①取代 ②加成 ③消去 ④酯化 ⑤加聚 ⑥水解 ⑦还原.其中能在有机化合物中引入-OH的反应类型有.
| A. | ①②③④⑤⑥ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | ①②⑥⑦ |

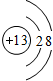 ,MgO的电子式
,MgO的电子式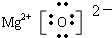 .
.