11.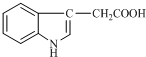 1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
 1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )| A. | 吲哚乙酸的分子式是C10H10NO2 | |
| B. | 吲哚乙酸苯环上的二氯代物共有四种(不考虑立体异构) | |
| C. | 吲哚乙酸可以发生取代反应、加成反应、氧化反应和还原反应 | |
| D. | 1 mol吲哚乙酸与足量氢气发生加成反应时,可以消耗5 mol H2 |
10.下列反应属于置换反应的是( )
| A. | Fe+CuSO4═FeSO4+Cu | B. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑ | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | NaOH+HCl═NaCl+H2O |
9.同温同压下,将四个容积相同的干燥圆底烧瓶中分别充满①NH3、②NO2、③混有空气的NH3、④混有空气的NO2进行喷泉实验.最后烧瓶内溶液的物质的量浓度(假设烧瓶内溶液不扩散)大小关系是( )
| A. | ①>②>③>④ | B. | ①=②=③=④ | C. | ①=②=③>④ | D. | ④>①=②=③ |
7.化学与社会、生产、生活密切相关,下列说法正确的是( )
| A. | 鲜花运输途中需喷洒高锰酸钾稀溶液,主要是为鲜花补充钾肥 | |
| B. | 牙膏中添加的Na3PO3F、NaF提供的氟离子浓度相等时,它们防治龋齿的作用相同 | |
| C. | 自来水厂用明矾净水,用Fe2(SO4)3或ClO2均能代替明矾净水 | |
| D. | 用石灰水或Na2SiO3溶液喷涂在树干上均可消灭树皮上的过冬虫卵 |
5.电离平衡是溶液化学中的重要内容,某化学兴趣小组拟以乙酸为例探究弱酸的性质.
(1)实验一:氢氧化钠标准溶液的配制.
现要配制0.1000mol/LNaOH标准溶液250mL,需要用到的玻璃仪器有玻璃棒、烧杯、胶头滴管和250毫升容量瓶,操作过程中如果没有将烧杯等的洗涤液一并转入容量瓶,在其它操作都正确的情况下,将该标准溶液用来滴定下列(2)中的未知浓度的乙酸溶液,将会使侧定的结果偏高(填“高”、“低”、“不影响”)
(2)实验二:现有一瓶乙酸溶液,常温下测定其中乙酸的电离平衡常数.设计实验方案,将待测物理量和对应的测定方法填写在表一中.
表一:
③上述实验中,如果在某温度时测得乙酸溶液的物质的量浓度为0.1000mol/L,pH=3,则在该温度时乙酸的电离平衡常数为1×10-5.
(3)实验三:探究酸的强弱对酸与镁条反应速率的影响.
①设计实验方案如表二,表二中c=2.0g.
表二:
②实验步骤:
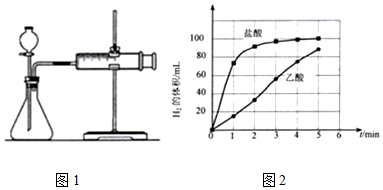
a)图1的装置中,在添加药品之前必须检查装置的气密性;
b)反应开始后,每隔1min记录一次生成H2的体积;
c)将所记录的欲据绘制成曲线图(图2).
③写出镁与乙酸溶液反应的离子方程式:Mg+2CH3COOH=Mg2++2CH3COO-+H2↑.
④描述0~5min盐酸与镁条反应的反应速率变化规律:醋酸与镁条反应的速率随时间变化不明显,盐酸与镁条反应开始阶段反应速率很快,一段时间后反应速率明显减小.
(1)实验一:氢氧化钠标准溶液的配制.
现要配制0.1000mol/LNaOH标准溶液250mL,需要用到的玻璃仪器有玻璃棒、烧杯、胶头滴管和250毫升容量瓶,操作过程中如果没有将烧杯等的洗涤液一并转入容量瓶,在其它操作都正确的情况下,将该标准溶液用来滴定下列(2)中的未知浓度的乙酸溶液,将会使侧定的结果偏高(填“高”、“低”、“不影响”)
(2)实验二:现有一瓶乙酸溶液,常温下测定其中乙酸的电离平衡常数.设计实验方案,将待测物理量和对应的测定方法填写在表一中.
表一:
| 待测物理量 | 测定方法 |
| ①乙酸溶液的物质的量浓度 | 量取25.00mL乙酸溶液于锥形瓶中,滴加指示剂,将0.1000mol/LNaOH标准溶液装入碱式滴定管,滴定至终点,记录数据.重复滴定2次. |
| ②H+的物质的量浓度 | 取适最乙酸溶液于烧杯中,用pH计或精密pH试纸测定溶液pH. |
(3)实验三:探究酸的强弱对酸与镁条反应速率的影响.
①设计实验方案如表二,表二中c=2.0g.
表二:
| 编号 | 酸的种类 | 酸的浓度(mol/L) | 酸的体积/mL | 镁条质量/g |
| l | 乙酸 | 0.5 | 17.0 | 2.0 |
| 2 | 盐酸 | 0.5 | 17.0 | c |

a)图1的装置中,在添加药品之前必须检查装置的气密性;
b)反应开始后,每隔1min记录一次生成H2的体积;
c)将所记录的欲据绘制成曲线图(图2).
③写出镁与乙酸溶液反应的离子方程式:Mg+2CH3COOH=Mg2++2CH3COO-+H2↑.
④描述0~5min盐酸与镁条反应的反应速率变化规律:醋酸与镁条反应的速率随时间变化不明显,盐酸与镁条反应开始阶段反应速率很快,一段时间后反应速率明显减小.
4.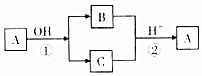 A是中学化学中常见的单质,B、C为化合物.它们有如图所示的转化关系(部分产物及反应条件省略).下列判断正确的是( )
A是中学化学中常见的单质,B、C为化合物.它们有如图所示的转化关系(部分产物及反应条件省略).下列判断正确的是( )
 A是中学化学中常见的单质,B、C为化合物.它们有如图所示的转化关系(部分产物及反应条件省略).下列判断正确的是( )
A是中学化学中常见的单质,B、C为化合物.它们有如图所示的转化关系(部分产物及反应条件省略).下列判断正确的是( )| A. | A可能是金属,也可能是非金属 | B. | A、B、C含有一种相同的元素 | ||
| C. | B、C的水溶液一定都呈碱性 | D. | 反应①②不一定都是氧化还原反应 |
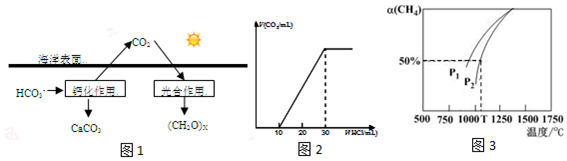
3.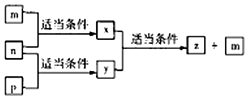 原子序数依次增大的短周期元素A、B、C、D分别位于不同的主族,m、p、n分别是元素A、B、C的单质,D的单质可与热水发生置换反应;x、y、z是由A、B、C组成的二元化合物,其中y、z是气体,且z可用于配制碳酸饮料.它们之间有如图转化关系,下列说法正确的是( )
原子序数依次增大的短周期元素A、B、C、D分别位于不同的主族,m、p、n分别是元素A、B、C的单质,D的单质可与热水发生置换反应;x、y、z是由A、B、C组成的二元化合物,其中y、z是气体,且z可用于配制碳酸饮料.它们之间有如图转化关系,下列说法正确的是( )
 原子序数依次增大的短周期元素A、B、C、D分别位于不同的主族,m、p、n分别是元素A、B、C的单质,D的单质可与热水发生置换反应;x、y、z是由A、B、C组成的二元化合物,其中y、z是气体,且z可用于配制碳酸饮料.它们之间有如图转化关系,下列说法正确的是( )
原子序数依次增大的短周期元素A、B、C、D分别位于不同的主族,m、p、n分别是元素A、B、C的单质,D的单质可与热水发生置换反应;x、y、z是由A、B、C组成的二元化合物,其中y、z是气体,且z可用于配制碳酸饮料.它们之间有如图转化关系,下列说法正确的是( )| A. | D的单质起火燃烧时可用z作灭火剂 | B. | 元素的非金属性:C>A>B | ||
| C. | B、C与A形成化合物的沸点:C>B | D. | 原子半径:D>B>C>A |
2.下列有关实验操作、现象和解释或结论都正确的是( )
0 162411 162419 162425 162429 162435 162437 162441 162447 162449 162455 162461 162465 162467 162471 162477 162479 162485 162489 162491 162495 162497 162501 162503 162505 162506 162507 162509 162510 162511 162513 162515 162519 162521 162525 162527 162531 162537 162539 162545 162549 162551 162555 162561 162567 162569 162575 162579 162581 162587 162591 162597 162605 203614
| 选项 | 操 作 | 现 象 | 解释或结论 |
| A | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大Cl-浓度,平衡逆向移动 |
| B | 将氯化铝溶液蒸干 | 析出白色固体 | 白色固体是氯化铝 |
| C | 向某溶液中滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| D | 石蕊试液中通入氯气 | 溶液先变红后红色褪去 | 氯气与水反应产生了酸和漂白性物质 |
| A. | A | B. | B | C. | C | D. | D |