7.下列比较或归纳一定正确的是( )
| A. | 离子半径:阴离子>阳离子 | B. | 酸性:HClO4>H2SO4 | ||
| C. | 熔沸点:共价化合物>离子化合物 | D. | 稳定性:PH3>NH3 |
6.硫酸铜晶体中结晶水含量测定,需用的仪器有( )
| A. | 容量瓶 | B. | 分液漏斗 | C. | 干燥器 | D. | 滴定管 |
5.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1L1mol•L-1的FeCl3溶液中Fe3+的数目为NA | |
| B. | 32g甲烷中含有2NA个C-H键 | |
| C. | 1molNH2-含有10NA个电子 | |
| D. | 1molNa2O2与足量CO2反应.转移电子数为2NA |
4.下列关于有机化学实验的说法正确的是( )
| A. | 除去苯中的甲苯,可使用酸性 KMnO4和 NaOH,然后分液 | |
| B. | 除去乙醇中混有的少量乙酸,加 NaOH 溶液,然后分液 | |
| C. | 检验溴乙烷中溴元素,直接加入硝酸银溶液生成浅黄色沉淀 | |
| D. | 实验室制备乙烯时,产生的气体直接通入溴水,溴水褪色,证明有乙烯生成 |
3.海带提碘实验中,不会用到的装置是( )
| A. | 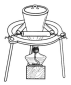 | B. |  | C. | 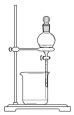 | D. | 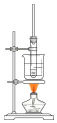 |
2.下列说法或实验操作不正确的是( )
| A. | 配制10%的ZnSO4溶液,将l0gZnSO4溶解于90g水中 | |
| B. | 用四氯化碳萃取碘水中的碘时,将碘的四氯化碳溶液从分液漏斗下口放出 | |
| C. | NaCl溶液蒸发结晶时,蒸发血中有晶体析出并剩余少量液体时即停止加热 | |
| D. | 检验蔗糖水解产物具有还原性时,先向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的银氨溶液,并水浴加热 |
1.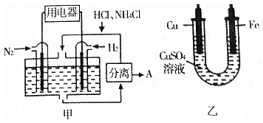 如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.
如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.
下列说法中正确的是( )
 如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.
如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl-NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜.下列说法中正确的是( )
| A. | 通入H2-极与图乙中的铜电极相连 | |
| B. | 电池工作一段时间后,溶液pH减少1 | |
| C. | 当消耗0.025molN2时,则铁电极增重1.6g | |
| D. | 通入N2-端的电极反应式为:N2+8H++6e-═2NH4+ |
20.下列说法正确的是( )
| A. | 淀粉水解的最终产物是麦芽糖 | |
| B. | 丙烯分子中三个碳原子处于同一直线上 | |
| C. | 二氯甲烷只有一种结构,可证明甲烷是正四面体构型 | |
| D. | 符合分子式为C4H10O能与金属钠反应的有机物有3种 |
19.下列有关实验仪器使用方法或实验操作正确的是( )
| A. | 酸式滴定管和容量瓶在使用前都要用相应溶液润洗 | |
| B. | 常温下,向Fe和Cu中分别加人浓硝酸,可以比较Fe和Cu的金属活动性强弱 | |
| C. | 制取无水MgCl2固体,可将MgCl2溶液置于蒸发皿中加热蒸干 | |
| D. | 分离乙酸乙酯和饱和Na2CO3溶液可用分液的方法 |
18.资料显示“O2的氧化性随溶液pH的增大逐渐减弱”.某兴趣小组探究不同条件下KI与O2的反应.实验如下.
(1)实验②中生成I2的离子方程式是4I-+O2+4H+=2I2+2H2O.
(2)实验③的目的是验证Cl-是否影响KI与O2的反应.
(3)实验④比②溶液颜色浅的原因是其他条件相同时,CH3COOH是弱电解质,溶液中c(H+)较盐酸小,O2的氧化性减弱.
(4)为进一步探究KI与O2的反应,用上表中的装置继续进行实验:
I.对于实验⑥的现象.甲同学提出猜想“pH=10时O2不能氧化I-”,设计了下列装置进行实验,验证猜想.
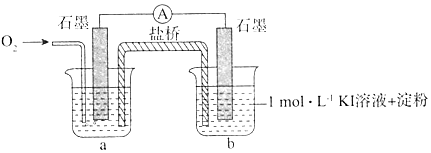
i.烧杯a中的溶液为pH=10的KOH溶液.
ii.实验结果表明,此猜想不成立.支持该结论的实验现象是:通入O2后,电流表指针偏转,烧杯b的溶液颜色变深.
Ⅱ.乙同学向pH=10的KOH溶液(含淀粉)中滴加碘水,溶液先变蓝后迅速褪色.经检测褪色后的溶液中含有IO3-,褪色的原因是(用离子方程式表示)3I2+6OH-=IO3-+5I-+3H2O.
(5)该小组同学对实验过程进行了整体反恩.推测实验①的现象产生的原因可能是中性条件下,O2的氧化性比较弱,该反应速率慢,短时间内难以生成“一定量”碘单质使溶液颜色发生变化;实验⑥的现象产生的原因可能是pH=10的KOH溶液中I-被氧化生成I2,I2迅速发生歧化反应变为IO3-和I-.
0 162385 162393 162399 162403 162409 162411 162415 162421 162423 162429 162435 162439 162441 162445 162451 162453 162459 162463 162465 162469 162471 162475 162477 162479 162480 162481 162483 162484 162485 162487 162489 162493 162495 162499 162501 162505 162511 162513 162519 162523 162525 162529 162535 162541 162543 162549 162553 162555 162561 162565 162571 162579 203614
| 装置 | 烧杯中的液体 | 现象(5分钟后) |
 | ①2mL1mol/LKl溶液+5滴淀粉 | 无明显变化 |
| ②2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L HCl | 溶液变蓝 | |
| ③2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L KCl | 无明显变化 | |
| ④2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L CH3COOH | 溶液变蓝,颜色较②浅 |
(2)实验③的目的是验证Cl-是否影响KI与O2的反应.
(3)实验④比②溶液颜色浅的原因是其他条件相同时,CH3COOH是弱电解质,溶液中c(H+)较盐酸小,O2的氧化性减弱.
(4)为进一步探究KI与O2的反应,用上表中的装置继续进行实验:
| 烧杯中的液体 | 现象(5小时后) |
| ⑤2mLpH=8.5混有KOH的1mol/L KI溶液+5滴淀粉 | 溶液才略变蓝 |
| ⑥2mLpH=10混有KOH的1mol/L KI溶液+5滴淀粉 | 无明显变化 |

i.烧杯a中的溶液为pH=10的KOH溶液.
ii.实验结果表明,此猜想不成立.支持该结论的实验现象是:通入O2后,电流表指针偏转,烧杯b的溶液颜色变深.
Ⅱ.乙同学向pH=10的KOH溶液(含淀粉)中滴加碘水,溶液先变蓝后迅速褪色.经检测褪色后的溶液中含有IO3-,褪色的原因是(用离子方程式表示)3I2+6OH-=IO3-+5I-+3H2O.
(5)该小组同学对实验过程进行了整体反恩.推测实验①的现象产生的原因可能是中性条件下,O2的氧化性比较弱,该反应速率慢,短时间内难以生成“一定量”碘单质使溶液颜色发生变化;实验⑥的现象产生的原因可能是pH=10的KOH溶液中I-被氧化生成I2,I2迅速发生歧化反应变为IO3-和I-.