5.有机物E的名称是( )
| A. | 丁烷 | B. | 2-甲基丙烷 | C. | 1-甲基丙烷 | D. | 甲烷 |
4.下列反应中,基本反应类型正确的是( )
| A. | 丙烯和氯气光照--取代 | |
| B. | 乙烯和溴水的反应--氧化 | |
| C. | 乙烯使酸性高锰酸钾溶液褪色--加成 | |
| D. | 乙烯水化法制乙醇--取代 |
3.关于如图所示装置的叙述,正确的是( )


| A. | 铜是阳极,铜片上有气泡产生 | B. | 溶液由无色逐渐变成蓝色 | ||
| C. | 电流由锌片流向铜片 | D. | 锌片被氧化 |
2.以下命题符合化学变化规律的是( )
| A. | 金属铜制成纳米铜 | B. | 把水变成汽油 | ||
| C. | 热核聚变把氢原子变成氦原子 | D. | 干冰变成原子晶体 |
1.将纯锌片和纯铜片按如图所方式插入同浓度的稀硫酸中,一段时间后,以下叙述正确的是( )

| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中化学能转化成了电能 | ||
| C. | 甲中铜片是负极 | D. | 乙中铜片是正极 |
20.常温下,有下列四种溶液:①0.1 mol/L NaOH溶液 ②pH=11 NaOH溶液 ③0.1 mol/L CH3COOH溶液 ④pH=3 CH3COOH溶液 ⑤pH=3 HCl溶液,下列说法正确的是( )
| A. | 由水电离出H+的浓度c(H+):①>③ | |
| B. | 将等体积的④、⑤分别加蒸馏水稀释至pH=6,加入水的体积:④>⑤ | |
| C. | ①与③混合,若溶液pH=7,则体积:V(NaOH)>V(CH3COOH) | |
| D. | 将②与④等体积混合,得到的溶液pH>7 |
19.在标准状况下进行甲、乙、丙三组实验.三组实验均各取20mL同浓度的盐酸,加入同一种镁铝合金粉末,产生气体,有关数据见表:
请回答下列问题:
(1)要算出盐酸的物质的量浓度,题中作为计算依据的数据是乙或丙,求得的盐酸的物质的量浓度为1.5mol/L.
(2)求合金中Mg、Al的物质的量之比,题中可作为计算依据的数据是甲,求得的Mg、Al物质的量之比为1:1.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(1)要算出盐酸的物质的量浓度,题中作为计算依据的数据是乙或丙,求得的盐酸的物质的量浓度为1.5mol/L.
(2)求合金中Mg、Al的物质的量之比,题中可作为计算依据的数据是甲,求得的Mg、Al物质的量之比为1:1.
18.下列说法是否正确( )
①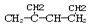 名称是1,3-二甲基-2-丁烯
名称是1,3-二甲基-2-丁烯
②相对分子质量相同的两种有机物一定是同分异构体
③烯烃各同系物中碳的质量分数都相等
④从煤焦油中分离出苯、甲苯、二甲苯等有机物的过程为化学变化
⑤在相同条件下,燃烧等质量的C2H4和苯,乙烯消耗O2的量多
⑥苯乙炔中最多有6个原子在同一条直线上.
①
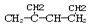 名称是1,3-二甲基-2-丁烯
名称是1,3-二甲基-2-丁烯②相对分子质量相同的两种有机物一定是同分异构体
③烯烃各同系物中碳的质量分数都相等
④从煤焦油中分离出苯、甲苯、二甲苯等有机物的过程为化学变化
⑤在相同条件下,燃烧等质量的C2H4和苯,乙烯消耗O2的量多
⑥苯乙炔中最多有6个原子在同一条直线上.
| A. | 都不正确 | B. | ③⑤⑥正确 | C. | ②④⑥正确 | D. | ①③⑥正确 |
17.在25℃、1.01×105Pa下,将33gCO2通入到1000ml1.0mol•L-1的NaOH溶液中充分反应,放出xkJ热量.在该条件下1molCO2通入到2L1.0mol•L-1的NaOH溶液中充分反应,放出ykJ热量,则CO2与NaOH反应生成NaHCO3的热化学反应方程式为( )
0 162281 162289 162295 162299 162305 162307 162311 162317 162319 162325 162331 162335 162337 162341 162347 162349 162355 162359 162361 162365 162367 162371 162373 162375 162376 162377 162379 162380 162381 162383 162385 162389 162391 162395 162397 162401 162407 162409 162415 162419 162421 162425 162431 162437 162439 162445 162449 162451 162457 162461 162467 162475 203614
| A. | CO2(g)+NaOH(aq)=NaHCO3(aq)△H=-(2y-x)kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)=NaHCO3(aq)△H=-(4x-y)kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)=NaHCO3(aq)△H=-1/2(4x-y)kJ•mol-1 | |
| D. | CO2(g)+NaOH(aq)=NaHCO3(aq)△H=-(8x-2y)kJ•mol-1 |