题目内容
20.常温下,有下列四种溶液:①0.1 mol/L NaOH溶液 ②pH=11 NaOH溶液 ③0.1 mol/L CH3COOH溶液 ④pH=3 CH3COOH溶液 ⑤pH=3 HCl溶液,下列说法正确的是( )| A. | 由水电离出H+的浓度c(H+):①>③ | |
| B. | 将等体积的④、⑤分别加蒸馏水稀释至pH=6,加入水的体积:④>⑤ | |
| C. | ①与③混合,若溶液pH=7,则体积:V(NaOH)>V(CH3COOH) | |
| D. | 将②与④等体积混合,得到的溶液pH>7 |
分析 A.0.1mol/LNaOH溶液中,由水电离出的c(H+)为10-13mol/L,0.1mol/L CH3COOH溶液,c(H+)<0.1mol/L,则由水电离出的c(H+)大于10-13mol/L;
B. ④pH=3 CH3COOH溶液 ⑤pH=3 HCl溶液,稀释相同的倍数,盐酸的PH值变化大,所以稀释到相同的PH,盐酸加水的体积小;
C.①与③混合,若溶液pH=7,c(H+)=c(OH-),结合电荷守恒分析;
D.②与④等体积混合,醋酸钠与醋酸的混合溶液,醋酸电离大于醋酸根离子水解,所以溶液呈酸性.
解答 解:A.0.1mol/LNaOH溶液中,由水电离出的c(H+)为10-13mol/L,0.1mol/L CH3COOH溶液,c(H+)<0.1mol/L,则由水电离出的c(H+)大于10-13mol/L,所以由水电离出的c(H+)为①<③,故A错误;
B.④pH=3 CH3COOH溶液 ⑤pH=3 HCl溶液,稀释相同的倍数,盐酸的PH值变化大,所以稀释到相同的PH,盐酸加水的体积小,所以将等体积的④、⑤分别加蒸馏水稀释至pH=6,加入水的体积:④>⑤,故B正确;
C.①与③混合,若溶液pH=7,c(H+)=c(OH-),由电荷守恒可知c(CH3COO-)=c(Na+),则为醋酸和醋酸钠的混合液,醋酸浓度大于NaOH溶液的浓度,满足醋酸过量即可,所以V(NaOH)≤V(CH3COOH),或V(NaOH)>V(CH3COOH)也可能,故C错误;
D.②与④等体积混合,醋酸钠与醋酸的混合溶液,醋酸电离大于醋酸根离子水解,所以溶液呈酸性,所以得到的溶液pH<7,故D错误;
故选B.
点评 本题考查酸碱混合pH的判断及溶液酸碱性的分析,选项C为解答的难点,注意酸碱混合时pH与浓度的关系、电离与水解的关系等即可解答,题目难度较大.

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案| A. | 丁烷 | B. | 2-甲基丙烷 | C. | 1-甲基丙烷 | D. | 甲烷 |
| A. | 1:1:1 | B. | 1:1:2 | C. | 1:2:2 | D. | 4:3:2 |
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. | CH3-CH2-CH=CH2 3-丁烯 | ||
| C. | 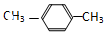 ,对二甲苯 ,对二甲苯 | D. | 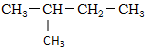 ,3-甲基丁烷 ,3-甲基丁烷 |
| A. | 23gNa与氧气充分燃烧,转移的电子数为NA | |
| B. | 1mol甲醇中含有的共价键数为4NA | |
| C. | 46gNO2和N2O4的混合气体含有的原子数为2NA | |
| D. | 标准状况下,22.4L氨水含有NH3分子数为NA |