7.已知断裂1mol H2(g)中的H-H键需要吸收436.4KJ的能量,断裂1mol O2(g)中的共价键需要吸收498KJ的能量,生成H2O(g)中的1mol H-O键能放出462.8KJ的能量.下列说法正确的是( )
| A. | 断裂1 mol H2O中的化学键需要吸收925.6 KJ的能量 | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H=-480.4 KJ•mol-1 | |
| C. | 2H2O(l)═2H2(g)+O2(g)△H=471.6 KJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-240.2KJ•mol-1 |
6.W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,下列说法不正确的是( )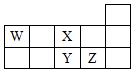

| A. | Z、Y、X的原子半径依次减小,非金属性依次降低 | |
| B. | Z、Y、W的最高价氧化物对应水化物的酸性依次降低 | |
| C. | WH4与Z元素的单质在一定条件下可能发生化学反应 | |
| D. | W的位置是第2周期、第ⅣA族 |
5.下列物质放入水中,会显著放热的是( )
| A. | 食盐 | B. | 蔗糖 | C. | 酒精 | D. | 生石灰 |
4.下列表示不正确的是( )
| A. | CO2的电子式 | B. | Cl2的结构式:Cl-Cl | ||
| C. | CH4的球棍模型 | D. | Clˉ离子的结构示意图  |
3. 世某著名学术刊物近期介绍了一种新型中温全瓷铁--空气电池,如图所示.下列有关该电池放电时的说法正确的是( )
世某著名学术刊物近期介绍了一种新型中温全瓷铁--空气电池,如图所示.下列有关该电池放电时的说法正确的是( )
 世某著名学术刊物近期介绍了一种新型中温全瓷铁--空气电池,如图所示.下列有关该电池放电时的说法正确的是( )
世某著名学术刊物近期介绍了一种新型中温全瓷铁--空气电池,如图所示.下列有关该电池放电时的说法正确的是( )| A. | a极发生还原反应 | |
| B. | 正极的电极反应式为FeOx+2xe-═Fe+xO2- | |
| C. | 若有22.4L(标准状况)空气参与反应,则电路中转移4mol电子 | |
| D. | 铁表面发生的反应为xH2O(g)+Fe═FeOx+xH2 |
2.某固体粉末X由两种物质组成,为确定该固体粉末的成分,某同学进行了以下实验:
①将固体粉末X加入足量稀盐酸中,有红色不溶物出现,同时有气泡产生;
②取①中的溶液加适量的H2O2溶液,再滴入KSCN溶液,溶液显红色
则该固体粉末X可能为( )
①将固体粉末X加入足量稀盐酸中,有红色不溶物出现,同时有气泡产生;
②取①中的溶液加适量的H2O2溶液,再滴入KSCN溶液,溶液显红色
则该固体粉末X可能为( )
| A. | Zn、CuO | B. | Fe、Al2O3 | C. | Fe、CuO | D. | Cu、FeO |
20.实验室制取乙酸乙酯:CH3COOH+C2H5OH $?_{△}^{浓硫酸}$CH3COOC2H5+H2O.下列操作或装置能达到实验目的是( )
| A | B | C | D |
 | 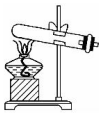 |  |  |
| 混合反应物 | 生成乙酸乙酯 | 收集乙酸乙酯 | 分离乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
19.某研究小组为探究Cu的化学性质及溶液环境对反应的影响,设计并完成了下列实验.
Ⅰ.探究Cu的化学性质
(1)根据化合价分析,在化学反应中铜主要体现出的化学性质是还原性.
(2)写出铜与稀硝酸反应的离子方程式3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O.
(3)向实验①的集气瓶中加水,随着水量的增加,溶液由黄色变为绿色,最后变为蓝色.
【查阅资料】
ⅰ.黄色与蓝色混合呈现绿色.
ⅱ.溶液中存在如下平衡:[Cu(H2O)4]2++4Cl-?[CuCl4]2-+4H2O
利用化学用语和文字解释溶液颜色变化的原因:[CuCl4]2-+4H2O?[Cu(H2O)4]2++4 Cl-,加水过程中,平衡正向移动,随着[Cu(H2O)4]2+的增加,溶液由黄色变为绿色,最后变为蓝色.
(4)反应③中溶液颜色无明显变化,是因为中性环境下反应很难进行.铜表面黑色的物质为CuO,同时有MnO2生成,则中性环境下反应很难进行的原因是:生成的CuO覆盖在铜的表面阻止反应继续.
Ⅱ.探究溶液环境对反应的影响
为进一步研究酸碱性对铜与0.1mol/L KMnO4溶液反应的影响,设计如图实验: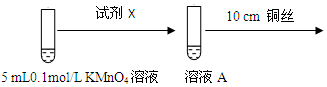
(1)探究酸性条件下反应时,试剂X是.溶液颜色变浅能否说明铜与0.1mol/L KMnO4溶液在酸性条件下发生了反应,理由是如果加入H2SO4溶液的体积是1 mL,对比碱性条件下的实验现象,则能说明发生了反应,如果加入H2SO4溶液的体积是大于1 mL,则有可能是稀释作用导致的溶液颜色变浅.
(2)对于铜与0.1mol/L KMnO4溶液在碱性环境下的反应提出如下假设:
假设Ⅰ:0.1mol/L KMnO4溶液在碱性环境下不能将铜氧化;
假设Ⅱ:0.1mol/L KMnO4溶液在碱性环境下与铜反应较慢.
设计实验验证:
将铜丝紧密缠绕在碳棒上放入碱性的溶液A中,溶液很快由紫红色变为深绿色、.一段时间后,溶液变为浅蓝绿色,试管底部出现棕褐色粉末(MnO2).①反应加快的原因是发生了电化学腐蚀,其正极发生的电极反应式为:MnO4-+e-→MnO42-、MnO42-+2e-+2H2O=MnO2+4OH-.
②通过上述实验得出结论.
Ⅰ.探究Cu的化学性质
| 实验 | 试剂1 | 试剂2 | 操作及现象 |
| ① | 铜丝 | 氯气 | 将加热后的铜丝伸入盛有氯气的集气瓶中,产生棕黄色的烟 |
| ② | 稀硝酸 | 产生无色气体,遇空气变为红棕色 | |
| ③ | 0.1mol/LKMnO4溶液 | 加热后,铜丝表面有黑色物质,溶液颜色无明显变化 |
(2)写出铜与稀硝酸反应的离子方程式3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O.
(3)向实验①的集气瓶中加水,随着水量的增加,溶液由黄色变为绿色,最后变为蓝色.
【查阅资料】
ⅰ.黄色与蓝色混合呈现绿色.
ⅱ.溶液中存在如下平衡:[Cu(H2O)4]2++4Cl-?[CuCl4]2-+4H2O
利用化学用语和文字解释溶液颜色变化的原因:[CuCl4]2-+4H2O?[Cu(H2O)4]2++4 Cl-,加水过程中,平衡正向移动,随着[Cu(H2O)4]2+的增加,溶液由黄色变为绿色,最后变为蓝色.
(4)反应③中溶液颜色无明显变化,是因为中性环境下反应很难进行.铜表面黑色的物质为CuO,同时有MnO2生成,则中性环境下反应很难进行的原因是:生成的CuO覆盖在铜的表面阻止反应继续.
Ⅱ.探究溶液环境对反应的影响
为进一步研究酸碱性对铜与0.1mol/L KMnO4溶液反应的影响,设计如图实验:

| 环境 | 反应现象 |
| 酸性 | 溶液紫红色变浅 |
| 碱性(1mL 1mol/L NaOH溶液) | 无明显现象 |
(2)对于铜与0.1mol/L KMnO4溶液在碱性环境下的反应提出如下假设:
假设Ⅰ:0.1mol/L KMnO4溶液在碱性环境下不能将铜氧化;
假设Ⅱ:0.1mol/L KMnO4溶液在碱性环境下与铜反应较慢.
设计实验验证:
将铜丝紧密缠绕在碳棒上放入碱性的溶液A中,溶液很快由紫红色变为深绿色、.一段时间后,溶液变为浅蓝绿色,试管底部出现棕褐色粉末(MnO2).①反应加快的原因是发生了电化学腐蚀,其正极发生的电极反应式为:MnO4-+e-→MnO42-、MnO42-+2e-+2H2O=MnO2+4OH-.
②通过上述实验得出结论.
18.X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如表所示:
请回答下列问题:
(1)W位于周期表中第三周期,第ⅦA族;
(2)X可形成双原子分子,其分子的电子式是 ;Y和氢元素形成的10电子微粒中常见+1价阳离子为H3O+(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子的水解方程式HS-+H2O?H2S+OH-.
;Y和氢元素形成的10电子微粒中常见+1价阳离子为H3O+(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子的水解方程式HS-+H2O?H2S+OH-.
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式2S2Cl2+2H2O═3S↓+SO2↑+4HCl.
(4)将0.20molZY2和0.10molO2充入一个固定容积为5L的密闭容器中,在一定温度并有催化剂存在下,进行反应,经半分钟达到平衡,测得溶液中含YZ30.18mol,则v(O2)=0.036mol/(L•min);若温度不变,继续通入0.20molYZ2和0.10molO2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.36mol<n(YZ3)<0.40mol.
0 162159 162167 162173 162177 162183 162185 162189 162195 162197 162203 162209 162213 162215 162219 162225 162227 162233 162237 162239 162243 162245 162249 162251 162253 162254 162255 162257 162258 162259 162261 162263 162267 162269 162273 162275 162279 162285 162287 162293 162297 162299 162303 162309 162315 162317 162323 162327 162329 162335 162339 162345 162353 203614
| X | Y | |
| Z | W |
(1)W位于周期表中第三周期,第ⅦA族;
(2)X可形成双原子分子,其分子的电子式是
 ;Y和氢元素形成的10电子微粒中常见+1价阳离子为H3O+(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子的水解方程式HS-+H2O?H2S+OH-.
;Y和氢元素形成的10电子微粒中常见+1价阳离子为H3O+(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子的水解方程式HS-+H2O?H2S+OH-.(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式2S2Cl2+2H2O═3S↓+SO2↑+4HCl.
(4)将0.20molZY2和0.10molO2充入一个固定容积为5L的密闭容器中,在一定温度并有催化剂存在下,进行反应,经半分钟达到平衡,测得溶液中含YZ30.18mol,则v(O2)=0.036mol/(L•min);若温度不变,继续通入0.20molYZ2和0.10molO2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.36mol<n(YZ3)<0.40mol.
 .
.