15.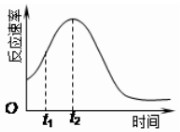 某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种.
某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种.
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
(1)猜想Ⅱ可能是:生成的Mn2+在反应中起到催化剂的作用,加快了反应速率
(2)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
 某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种.
某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种.猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
(1)猜想Ⅱ可能是:生成的Mn2+在反应中起到催化剂的作用,加快了反应速率
(2)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
| 试管A | 试管B | |
| 加入试剂 | 2mL0.1mol/L H2C2O4溶液、1mL 0.05mol/L 酸性KMnO4 | 2mL0.1mol/L H2C2O4溶液、1mL 0.05mol/L 酸性KMnO4,少量MnSO4(s)固体(填物质名称) |
| 实验现象(褪色时间) | 褪色时间10min | 褪色时间<10min(选填“<”“>”或“=”) |
| 结论 | 猜想Ⅱ正确 | |
11.将质量分数为35%的氨水与质量分数为5%的氨水等体积混合后,所得氨水的质量分数为( )
| A. | 等于20% | B. | 大于20% | C. | 小于20% | D. | 无法计算 |
8.化学学习小组进行如下实验.
【探究反应速率的影响因素】设计了如下的方案并记录实验结果(忽略溶液混合体积变 化).限选试剂和仪器:0.20mol/LH2C2O4溶液、0.010mol/LKMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
(1)上述实验①②是探究温度对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则 a 为1.0;乙是实验需要测量的物理量,则表 格中“乙”应填写t 溶液褪色时间/s.
【测定 H2C2O4•xH2O 中 x 值】已知:M(H2C2O4)=90g/mol
①称取 1.260g 纯草酸晶体,将其酸制成 100.00mL 水溶液为待测液.
②取 25.00mL 待测液放入锥形瓶中,再加入适的稀 H2SO4
③用浓度为 0.05000mol•L-1 的 KMnO 标准溶液进行滴定;
(2)请写出与滴定有关反应的离子方程式6H++5H2C2O4+2MnO4-=2Mn2++10CO2↑+8H2O
(3)某学生的滴定方式(夹持部分略去)如图1,最合理的是b(选填 a、b).
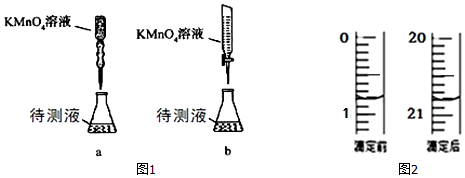
(4)由图2可知消耗 KMnO4溶液体积为20.00mL;
(5)滴定过程中眼睛应注视锥形瓶中颜色变色;
(6)通过上述数据,求得 x=2.以标准 KMnO4溶液滴定样品溶液的浓度,未用标准 KMnO4溶液润洗滴定管,引起实验结果偏大(偏大、偏小或没有影响).
0 162100 162108 162114 162118 162124 162126 162130 162136 162138 162144 162150 162154 162156 162160 162166 162168 162174 162178 162180 162184 162186 162190 162192 162194 162195 162196 162198 162199 162200 162202 162204 162208 162210 162214 162216 162220 162226 162228 162234 162238 162240 162244 162250 162256 162258 162264 162268 162270 162276 162280 162286 162294 203614
【探究反应速率的影响因素】设计了如下的方案并记录实验结果(忽略溶液混合体积变 化).限选试剂和仪器:0.20mol/LH2C2O4溶液、0.010mol/LKMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
| 物理量 | V(0.20mol/H2 | V(蒸馏水)/mL | V(0.010mol/L KMnO4溶液)/mL | T/℃ | 乙 |
| ① | 2.0 | 0 | 4.0 | 50 | |
| ② | 2.0 | 0 | 4.0 | 25 | |
| ③ | 1.0 | a | 4.0 | 25 |
【测定 H2C2O4•xH2O 中 x 值】已知:M(H2C2O4)=90g/mol
①称取 1.260g 纯草酸晶体,将其酸制成 100.00mL 水溶液为待测液.
②取 25.00mL 待测液放入锥形瓶中,再加入适的稀 H2SO4
③用浓度为 0.05000mol•L-1 的 KMnO 标准溶液进行滴定;
(2)请写出与滴定有关反应的离子方程式6H++5H2C2O4+2MnO4-=2Mn2++10CO2↑+8H2O
(3)某学生的滴定方式(夹持部分略去)如图1,最合理的是b(选填 a、b).

(4)由图2可知消耗 KMnO4溶液体积为20.00mL;
(5)滴定过程中眼睛应注视锥形瓶中颜色变色;
(6)通过上述数据,求得 x=2.以标准 KMnO4溶液滴定样品溶液的浓度,未用标准 KMnO4溶液润洗滴定管,引起实验结果偏大(偏大、偏小或没有影响).