20.现有下列六个转化,其中不能通过一步反应实现的是( )
①SiO2→Na2SiO3 ②S→SO3 ③NH3→N2
④CuO→Cu(OH)2 ⑤Cl2→NaClO ⑥SO2→H2SO4.
①SiO2→Na2SiO3 ②S→SO3 ③NH3→N2
④CuO→Cu(OH)2 ⑤Cl2→NaClO ⑥SO2→H2SO4.
| A. | ①②⑥ | B. | ②③④ | C. | ②④⑥ | D. | ②④ |
19.一定条件下反应A2(g)+B2(g)?2AB(g)达到平衡状态的标志是( )
| A. | 单位时间内生成n mol AB的同时生成n mol的B2 | |
| B. | 容器内的总压强不随时间而变化 | |
| C. | 2v(A2)正=v(AB)逆 | |
| D. | A2、B2、AB的反应速率之比为1:1:2的状态 |
16.下列对物质的量的理解,正确的是( )
| A. | 物质的量就是物质的数量 | |
| B. | 物质的量就是物质的摩尔质量 | |
| C. | 物质的量就是物质所含微粒数目的多少 | |
| D. | 物质的量是一种基本物理量 |
14. 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和图所示装置进行测定中和热的实验,得到表中的数据:
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和图所示装置进行测定中和热的实验,得到表中的数据:
试完成下列问题:
(1)填出图中实验仪器的名称A环形玻璃搅拌棒,B碎泡沫.
(2)实验时用A搅拌溶液的方法是上下搅动.不能用铜丝搅拌棒代替A的理由是铜传热快,防止热量损失.
(3)经数据处理,t2-t1=3.4℃.则该实验测得的中和热△H=-56.8kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].
(4)若将HCl溶液改为相同体积、相同浓度的醋酸,测得中和热为△H1=-Q KJ/mol,则Q与57.3的关系为:Q<57.3(填“<”、“>”或“=”),理由是醋酸边反应边电离,醋酸电离吸热.
 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和图所示装置进行测定中和热的实验,得到表中的数据:
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和图所示装置进行测定中和热的实验,得到表中的数据:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
(1)填出图中实验仪器的名称A环形玻璃搅拌棒,B碎泡沫.
(2)实验时用A搅拌溶液的方法是上下搅动.不能用铜丝搅拌棒代替A的理由是铜传热快,防止热量损失.
(3)经数据处理,t2-t1=3.4℃.则该实验测得的中和热△H=-56.8kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].
(4)若将HCl溶液改为相同体积、相同浓度的醋酸,测得中和热为△H1=-Q KJ/mol,则Q与57.3的关系为:Q<57.3(填“<”、“>”或“=”),理由是醋酸边反应边电离,醋酸电离吸热.
13.初中化学反应的基本类型包括:化合反应、分解反应、置换反应和复分解反应.下列反应中不属于这四种基本类型的是( )
| A. | CO2+H2O═H2CO3 | B. | CO+CuO═Cu+CO2 | ||
| C. | 2H2O═2H2↑+O2↑ | D. | FeS+H2SO4═FeSO4+H2S↑ |
12.下列关于过滤的叙述正确的是( )
0 161993 162001 162007 162011 162017 162019 162023 162029 162031 162037 162043 162047 162049 162053 162059 162061 162067 162071 162073 162077 162079 162083 162085 162087 162088 162089 162091 162092 162093 162095 162097 162101 162103 162107 162109 162113 162119 162121 162127 162131 162133 162137 162143 162149 162151 162157 162161 162163 162169 162173 162179 162187 203614
| A. | 过滤所需实验用品有漏斗、烧杯、玻璃棒、铁架台(带铁圈) | |
| B. | 过滤时把漏斗放在铁三脚架上 | |
| C. | 过滤时将玻璃棒斜靠在三层滤纸上 | |
| D. | 过滤时为了加快过滤速度,用玻璃棒搅拌过滤器中的液体 |
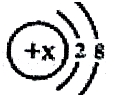 当x=8时,该粒子符号为O2-;当x=11时,该粒子符号为Na+;当x=13时,写出该粒子的硝酸盐的化学式为Al(NO3)3.
当x=8时,该粒子符号为O2-;当x=11时,该粒子符号为Na+;当x=13时,写出该粒子的硝酸盐的化学式为Al(NO3)3.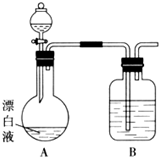 实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.
实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.


