题目内容
18.某简单离子的结构示意图可表示为: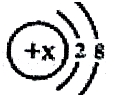 当x=8时,该粒子符号为O2-;当x=11时,该粒子符号为Na+;当x=13时,写出该粒子的硝酸盐的化学式为Al(NO3)3.
当x=8时,该粒子符号为O2-;当x=11时,该粒子符号为Na+;当x=13时,写出该粒子的硝酸盐的化学式为Al(NO3)3.
分析 根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子,以此解答该题.
解答 解:某简单粒子的结构示意图可表示为 .当X=8时,质子数=8,核外电子数=10,质子数<核外电子数,为氧离子,粒子的符号为O2-;
.当X=8时,质子数=8,核外电子数=10,质子数<核外电子数,为氧离子,粒子的符号为O2-;
当X=11时,质子数=11>核外电子数=10,为钠离子,其离子符号为:Na+;
当X=13时,质子数=13,核外电子数=10,质子数>核外电子数,为铝离子;与硝酸根化合形成的化合物为硝酸铝,铝元素显+3价,硝酸根显-1价,其化学式为:Al(NO3)3,
故答案为:O2-;Na+;Al(NO3)3.
点评 本题考查原子结构和元素的性质,为高频考点,侧重考查学生的分析能力和双基知识的掌握,注意把握原子核外电子的排布特点,难度不大.

练习册系列答案
相关题目
19.某澄清溶液中可能含有下列离子:K+、NH4+、Fe2+、Fe3+、Ba2+、SO42ˉ、HCO3ˉ、Clˉ,
为鉴别其中含有的离子,进行如下实验:
①用玻璃棒蘸取原溶液滴在pH试纸上,试纸显红色;
②另取少量原溶液加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀;
③取②中上层清液加入酸化的硝酸银溶液,生成白色沉淀.
下列关于原溶液的说法正确的是( )
为鉴别其中含有的离子,进行如下实验:
①用玻璃棒蘸取原溶液滴在pH试纸上,试纸显红色;
②另取少量原溶液加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀;
③取②中上层清液加入酸化的硝酸银溶液,生成白色沉淀.
下列关于原溶液的说法正确的是( )
| A. | 原溶液中一定存在SO42-和Cl- | |
| B. | 取③中滤液加入KSCN,溶液显红色,则原溶液一定有Fe3+ | |
| C. | 原溶液中一定不存在Ba2+和HCO3- | |
| D. | 为确定原溶液中是否含有K+,可通过焰色反应直接观察焰色是否为紫色来确定 |
13.初中化学反应的基本类型包括:化合反应、分解反应、置换反应和复分解反应.下列反应中不属于这四种基本类型的是( )
| A. | CO2+H2O═H2CO3 | B. | CO+CuO═Cu+CO2 | ||
| C. | 2H2O═2H2↑+O2↑ | D. | FeS+H2SO4═FeSO4+H2S↑ |
3.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液.下列说法正确的是( )
| A. | Zn为电池的正极 | |
| B. | 负极反应式为2FeO42-+10H++6e-═Fe2O3+5H2O | |
| C. | 该电池使用完不可随便丢弃,应深埋地下 | |
| D. | 电池工作时OH-向负极迁移 |
10.硫单质及其化合物在工农业生产中有着极其重要的应用.
(1)1molSO2与氯酸钠在酸性条件下反应生成消毒杀菌剂ClO2,该反应的氧化产物为Na2SO4,转移电子2mol.
(2)羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染.羰基硫的氢解和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g)+H2(g)=H2S(g)+CO(g)△H1=+7kJ/mol
②水解反应:COS(g)+H2O(g)=H2S(g)+CO2△H2
已知反应中相关的化学键键能数据如表:
则△H2=-35kJ/mol.
(3)H2S被足量氢氧化钠溶液吸收得到无色溶液A.溶液A在空气中长期放置发生反应,生成物之一为B.B与过氧化钠的结构和化学性质相似,B的溶液与稀硫酸反应的化学方程式为Na2S2+H2SO4=Na2SO4+S↓+H2S↑.
(4)经检测,某溶液中除SO42-外还有大量的Cl-、Br-、I-,若向2L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示.
分析后回答下列问题:
①a的值为0.15.
②当通入Cl2的体积为3.36L(标准状况下)时,溶液中发生反应的离子方程式为Cl2+2I-=2Cl-+I2.
此时溶液中Br-、I-的物质的量浓度分别为c(Br-)=0.75mol/L,c(I-)=0.5mol/L.
(1)1molSO2与氯酸钠在酸性条件下反应生成消毒杀菌剂ClO2,该反应的氧化产物为Na2SO4,转移电子2mol.
(2)羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染.羰基硫的氢解和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g)+H2(g)=H2S(g)+CO(g)△H1=+7kJ/mol
②水解反应:COS(g)+H2O(g)=H2S(g)+CO2△H2
已知反应中相关的化学键键能数据如表:
| 化学键 | C=O(CO2) | C=O(COS) | C=S | H-S | H-O |
| 键能(kJ/mol) | 803 | 742 | 577 | 339 | 465 |
(3)H2S被足量氢氧化钠溶液吸收得到无色溶液A.溶液A在空气中长期放置发生反应,生成物之一为B.B与过氧化钠的结构和化学性质相似,B的溶液与稀硫酸反应的化学方程式为Na2S2+H2SO4=Na2SO4+S↓+H2S↑.
(4)经检测,某溶液中除SO42-外还有大量的Cl-、Br-、I-,若向2L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示.
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(I-) | amol | 0 | 0 |
①a的值为0.15.
②当通入Cl2的体积为3.36L(标准状况下)时,溶液中发生反应的离子方程式为Cl2+2I-=2Cl-+I2.
此时溶液中Br-、I-的物质的量浓度分别为c(Br-)=0.75mol/L,c(I-)=0.5mol/L.
7.下列说法正确的是( )
| A. | 不粘锅的原料 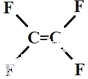 为烃类化合物 为烃类化合物 | |
| B. | 分子组成相差1个或若干个“CH2”原子团的有机物,互称为同系物 | |
| C. | 石油分馏是物理变化,煤的气化、液化是化学变化 | |
| D. | 聚乙烯塑料袋因有毒,不可以装食品 |
8.下列离子方程式书写正确的是( )
| A. | NaOH溶液与SO2反应,当n(NaOH):n(SO2)=4:3时,4OH-+3SO2═SO32-+2HSO3-+H2O | |
| B. | 碳酸氢镁中加过量氢氧化钠:Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O | |
| D. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
 )的一条路线如图:
)的一条路线如图: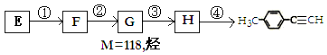
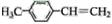 .
. 、
、 .
.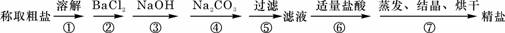
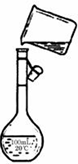 (5)为检验精盐纯度,需配制100mL 1mol/L NaCl溶液,右图是该同学转移溶液的示意图,图中的错误是未用玻璃棒引流
(5)为检验精盐纯度,需配制100mL 1mol/L NaCl溶液,右图是该同学转移溶液的示意图,图中的错误是未用玻璃棒引流