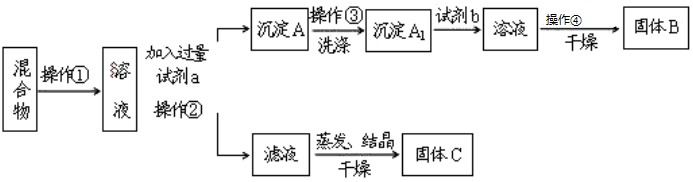
18.已知HI在催化剂作用下分解速率会加快,其能量随反应进程的变化如图所示.下列说法正确的是( )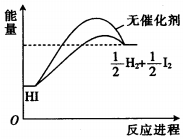

| A. | 加入催化剂,减小了反应的活化能 | |
| B. | 加入催化剂,可提高HI的平衡转化率 | |
| C. | 降低温度,HI的分解速率加快 | |
| D. | 反应物的总能量大于生成物的总能量 |
17.下列说法中不正确的是( )
| A. | 常温下,向100gNaOH饱和溶液中加入0.39gNa2O2固体,恢复到常温,NaOH溶液的物质的量浓度一定不变 | |
| B. | 向一恒容容器中充入lmolN2和lmolH2,在一定条件下反应并达到平衡.升温,再次达到平衡状态,N2的体积分数一定不变 | |
| C. | 向50mL0.55mol/L的NaOH溶液中加入50mL0.50mol/L的稀盐酸,测定中和热,继续加入6mL等浓度的稀盐酸,测定的中和热一定不变 | |
| D. | 将2.3gNa投入100mL水中,产生H2,若在反应前向水中加入100 mL煤油,则产生H2的速率一定不变 |
16.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 常温常压下,等质量的N2和CO气休的原子数均为2NA | |
| B. | 在反应KC1O4+8HCI=KCl+4Cl2↑+4H2O中,每生成4molCl2转移的电子数为8NA | |
| C. | 含有3mol离子的过氧化钠固体和足量的水反应,电子转移数为NA | |
| D. | 标准状况下,80gSO3中含3NA个氧原子,体积约为22.4L |
12.下列说法或表示法正确的是( )
| A. | 由“C(s,石墨)-→C(s,金刚石)△H=+119 kJ•mol-1”可知金刚石比石墨稳定 | |
| B. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ•mol-1 | |
| C. | 在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 | |
| D. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
11.S(单斜)和S(正交)是硫的两种同素异形体已知:
①S(单斜,s)+O2(g)=SO2(g)△H1=-297.16kJ•mol-1
②S(正交,s)+O2(g)=SO2(g)△H2=-296.83kJ•mol-1
③S(单斜,s)=S(正交,s)△H3
④S(正交,s)=S (g)△H4
⑤S(单斜,s)=S (g)△H5
下列说法正确的是( )
0 161978 161986 161992 161996 162002 162004 162008 162014 162016 162022 162028 162032 162034 162038 162044 162046 162052 162056 162058 162062 162064 162068 162070 162072 162073 162074 162076 162077 162078 162080 162082 162086 162088 162092 162094 162098 162104 162106 162112 162116 162118 162122 162128 162134 162136 162142 162146 162148 162154 162158 162164 162172 203614
①S(单斜,s)+O2(g)=SO2(g)△H1=-297.16kJ•mol-1
②S(正交,s)+O2(g)=SO2(g)△H2=-296.83kJ•mol-1
③S(单斜,s)=S(正交,s)△H3
④S(正交,s)=S (g)△H4
⑤S(单斜,s)=S (g)△H5
下列说法正确的是( )
| A. | 单斜硫转化为正交硫需要吸热 | B. | 单斜硫比正交硫稳定 | ||
| C. | △H4>△H5 | D. | △H4<0 |
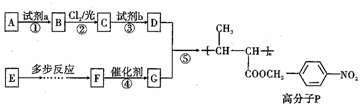
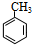 ,试剂a是浓硫酸和浓硝酸.
,试剂a是浓硫酸和浓硝酸.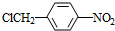 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$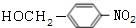 +NaCl.
+NaCl.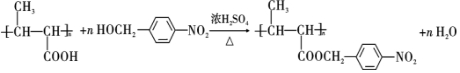 .
.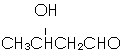 ,以E为起始原料.选用必要的无机试剂合成F,写出合成路线
,以E为起始原料.选用必要的无机试剂合成F,写出合成路线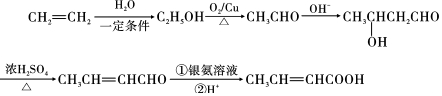 (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).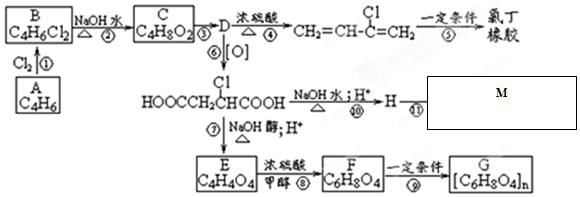

 用如图示装置制取少量乙酸乙酯.已知乙酸乙酯的沸点低于乙醇.请填空:
用如图示装置制取少量乙酸乙酯.已知乙酸乙酯的沸点低于乙醇.请填空: