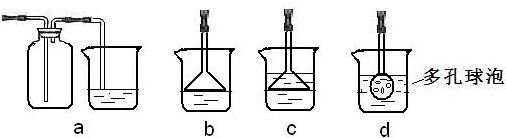
7.某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验:
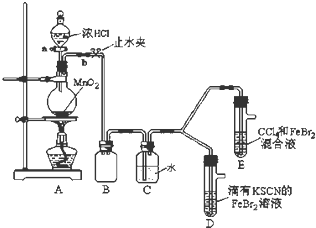
(1)①装置A中发生反应的离子方程式是MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
②整套实验装置存在一处明显的不足,请指出缺少尾气处理装置.
(2)用改正后的装置进行实验,实验过程如下:
(3)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化.
D装置中:红色慢慢褪去.
E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色.
为探究上述实验现象的本质,小组同学查得资料如下:
①请用平衡移动原理(结合上述资料)解释Cl2过量时D中溶液红色褪去的原因过量氯气和SCN-反应2SCN-+Cl2=2Cl-+(SCN)2,使SCN-浓度减小,
则使Fe3++3SCN-?Fe(SCN)3平衡向逆反应方向移动而褪色,现设计简单实验证明上述解释:取少量褪色后的溶液,滴加KSCN溶液(或FeCl3溶液)溶液,若溶液颜色变红色(或不变红),则上述解释是合理的.
②欲探究E中颜色变化的原因,设计实验如下:
用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生.请结合上述资料用两步方程式(离子或化学方程式不限定)解释仅产生白色沉淀原因BrCl+H2O=HBrO+H++Cl-、Ag++Cl-=AgCl↓.

(1)①装置A中发生反应的离子方程式是MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
②整套实验装置存在一处明显的不足,请指出缺少尾气处理装置.
(2)用改正后的装置进行实验,实验过程如下:
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯. | D装置中:溶液变红 E装置中:水层溶液变黄,振荡后,下层CCl4层无明显变化. | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为: Cl2>Br2>Fe3+ |
D装置中:红色慢慢褪去.
E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色.
为探究上述实验现象的本质,小组同学查得资料如下:
| ⅰ.Fe3++3SCN-?Fe(SCN)3 是一个可逆反应. ⅱ.(SCN)2性质与卤素单质类似.氧化性:Cl2>(SCN)2. ⅲ.Cl2和Br2反应生成BrCl,BrCl呈红色(略带黄色),沸点约5℃,它与水能发生水解反应,且该反应为非氧化还原反应. ⅳ.AgClO、AgBrO均可溶于水. |
则使Fe3++3SCN-?Fe(SCN)3平衡向逆反应方向移动而褪色,现设计简单实验证明上述解释:取少量褪色后的溶液,滴加KSCN溶液(或FeCl3溶液)溶液,若溶液颜色变红色(或不变红),则上述解释是合理的.
②欲探究E中颜色变化的原因,设计实验如下:
用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生.请结合上述资料用两步方程式(离子或化学方程式不限定)解释仅产生白色沉淀原因BrCl+H2O=HBrO+H++Cl-、Ag++Cl-=AgCl↓.
6.为了探究Cu(NO3)2的氧化性和热稳定性,某化学兴趣小组设计了如下实验.回答下列问题:
Ⅰ.Cu(NO3)2的氧化性
将光亮的铁丝伸入Cu(NO3)2溶液中,充分反应后将铁丝取出.为检验铁的氧化产物,进行如下实验.(可选用试剂:KSCN溶液、K3[Fe(CN)6]溶液、氯水)
(1)请完成下表:
【实验结论】Cu(NO3)2能将Fe氧化为Fe2+.
Ⅱ.Cu(NO3)2的热稳定性
用下图所示的实验装置A加热Cu(NO3)2固体,产生红棕色气体,试管中残留物为黑色固体,b中收集到无色气体.
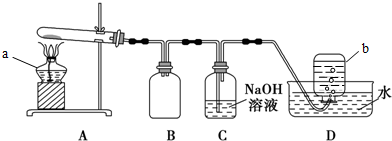
(2)仪器a的名称是酒精灯.装置B的作用是缓冲作用(或安全瓶等).
(3)【提出设想】b中收集到的无色气体可能是:i.氧气ⅱ.一氧化氮ⅲ.空气
【实验验证】该小组为验证上述设想,用玻璃片在水下盖住集气瓶口,并取出正放在桌面上,移开玻璃片后瓶口未发现颜色变化,将带火星的木条伸入集气瓶,未见复燃.
【实验结论】b中的气体是空气.根据上述实验结果,该小组得出了Cu(NO3)2固体加热分解的产物.请你帮助写出Cu(NO3)2加热分解的化学方程式2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑;C中反应的离子方程式4NO2+O2+4OH-═4NO3-+2H2O.
Ⅰ.Cu(NO3)2的氧化性
将光亮的铁丝伸入Cu(NO3)2溶液中,充分反应后将铁丝取出.为检验铁的氧化产物,进行如下实验.(可选用试剂:KSCN溶液、K3[Fe(CN)6]溶液、氯水)
(1)请完成下表:
| 操作 | 现象 | 结论 |
| 取少量溶液于试管中,加入KSCN溶液,振荡 | ①颜色无变化 | 不存在Fe3+ |
| 另取少量溶液于试管中,加入②K3[Fe(CN)6]溶液,振荡 | 蓝色沉淀 | 存在Fe2+ |
Ⅱ.Cu(NO3)2的热稳定性
用下图所示的实验装置A加热Cu(NO3)2固体,产生红棕色气体,试管中残留物为黑色固体,b中收集到无色气体.

(2)仪器a的名称是酒精灯.装置B的作用是缓冲作用(或安全瓶等).
(3)【提出设想】b中收集到的无色气体可能是:i.氧气ⅱ.一氧化氮ⅲ.空气
【实验验证】该小组为验证上述设想,用玻璃片在水下盖住集气瓶口,并取出正放在桌面上,移开玻璃片后瓶口未发现颜色变化,将带火星的木条伸入集气瓶,未见复燃.
【实验结论】b中的气体是空气.根据上述实验结果,该小组得出了Cu(NO3)2固体加热分解的产物.请你帮助写出Cu(NO3)2加热分解的化学方程式2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑;C中反应的离子方程式4NO2+O2+4OH-═4NO3-+2H2O.
16.有机物的结构可用“键线式”表示,下列有关键线式为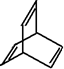 的有机物X的说法不正确的是( )
的有机物X的说法不正确的是( )
 的有机物X的说法不正确的是( )
的有机物X的说法不正确的是( )| A. | X的化学式为C8H8 | |
| B. | 有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为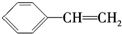 | |
| C. | X能使酸性高锰酸钾溶液褪色 | |
| D. | X与足量的H2在一定条件下反应可生成环状饱和烃Z,Z的一氯代物有4种 |
15.下列实验操作能达到实验目的是( )
| A. | 向生石灰中滴加浓氨水,可以制备氨气 | |
| B. | 用分液漏斗、烧杯、铁架台可以分离碘的四氯化碳溶液 | |
| C. | 用排饱和硝酸钾溶液的方法可以收集铜与浓硝酸产生的NO2 | |
| D. | 在含少量AlCl3的MgCl2溶液中加人过量MgO,过滤得到MgCl2溶液 |
14.据《俄新网》报道,萨彦斯克化工塑料厂一个生产二氯乙烷的高炉发生爆炸事故.该化工厂是俄罗斯一家最大的聚氯乙烯树脂生产厂家.下列有关二氯乙烷的说法不正确的是 ( )
0 161957 161965 161971 161975 161981 161983 161987 161993 161995 162001 162007 162011 162013 162017 162023 162025 162031 162035 162037 162041 162043 162047 162049 162051 162052 162053 162055 162056 162057 162059 162061 162065 162067 162071 162073 162077 162083 162085 162091 162095 162097 162101 162107 162113 162115 162121 162125 162127 162133 162137 162143 162151 203614
| A. | 二氯乙烷与四氯乙烷的同分异构体数相同 | |
| B. | 在光照条件下,乙烷与氯气反应不能制备纯净的二氯乙烷 | |
| C. | 二氯乙烷和硝酸银溶液反应产生白色沉淀 | |
| D. | 二氯乙烷发生消去反应可以得到乙炔 |