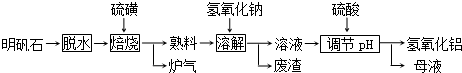
3.有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐.运用该原理生产铜和绿矾(FeSO4•7H2O)的流程如图:
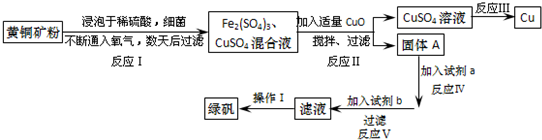
回答下列问题:
(1)已知:
加入CuO将溶液的pH调节到约为4,结合平衡移动原理解释该操作的原因Fe3+在溶液中存在存在平衡Fe3++3H2O?Fe(OH)3+3H+,加入CuO消耗溶液中的H+,使c(H+)减小,使Fe3+转化为Fe(OH)3沉淀而除去,不损耗铜离子且不引入杂质.
(2)写出能实现反应Ⅲ的化学方程式2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+2H2SO4+O2↑.
(3)试剂b为Fe.
(4)欲从滤液中获得绿矾晶体,操作Ⅰ应为浓缩、结晶、过滤.
(5)反应Ⅰ的化学方程式4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O.

回答下列问题:
(1)已知:
| Fe2+ | Cu2+ | Fe3+ | |
| 开始转化成氢氧化物沉淀时的pH | 7.6 | 4.7 | 2.7 |
| 完全转化成氢氧化物沉淀时的pH | 9.6 | 6.7 | 3.7 |
(2)写出能实现反应Ⅲ的化学方程式2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+2H2SO4+O2↑.
(3)试剂b为Fe.
(4)欲从滤液中获得绿矾晶体,操作Ⅰ应为浓缩、结晶、过滤.
(5)反应Ⅰ的化学方程式4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O.
6.香叶醛(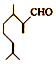 )是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯(
)是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯( ) 下列有关香叶醛与对异丙基甲苯的叙述正确的是( )
) 下列有关香叶醛与对异丙基甲苯的叙述正确的是( )
 )是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯(
)是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯( ) 下列有关香叶醛与对异丙基甲苯的叙述正确的是( )
) 下列有关香叶醛与对异丙基甲苯的叙述正确的是( )| A. | 两者互为同分异构体 | |
| B. | 两者均能与溴水发生加成反应 | |
| C. | 香叶醛的一种同分异构体可能是芳香醇 | |
| D. | 对异丙基甲苯的分子式为C10H14 |
5.钴及其化合物可应用与催化剂、电池、颜料与染料等.
(1)CoO是一种油漆添加剂,可通过反应①②制备.
①2Co(s)+O2(g)═2CoO(s)△H1=akJ•mol-1
②2CoCO3(s)═CoO(s)+CO2 (g)△H2=akJ•mol-1
则反应2Co(s)+O2(g)+2CO2(g)═2CoO3(s) 的△H=(a-2b)kJ•mol-1
(2)某锂电池的电解质可传导Li+,电池反应式为:LiC6+CoO2?C6+LiCoO2
①电池放电时,负极的电极反应式为,Li+向正极移动(填“正极”或“负极“).
②一种回收电极中Co元素的方法是:将LiCoO2与H2O2、H2SO4反应生成CoSO4.该反应的化学方程式为2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+4H2O+O2↑
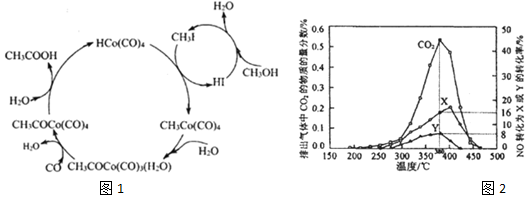
(3)BASF高压法制备醋酸采用钴碘催化循环过程如图1所示,该循环的总反应方程式为CO+CH3OH→CH3COOH(反应条件无需列出)
(4)某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx.不同温度下,将10mol模拟尾气(成分如图2所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如表
①380℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为N2O.
②实验过程中采用NO模拟NOx,而不采用NO2的原因是NO较NO2稳定,NO2气体中存在N2O4,不便于定量测定.

(1)CoO是一种油漆添加剂,可通过反应①②制备.
①2Co(s)+O2(g)═2CoO(s)△H1=akJ•mol-1
②2CoCO3(s)═CoO(s)+CO2 (g)△H2=akJ•mol-1
则反应2Co(s)+O2(g)+2CO2(g)═2CoO3(s) 的△H=(a-2b)kJ•mol-1
(2)某锂电池的电解质可传导Li+,电池反应式为:LiC6+CoO2?C6+LiCoO2
①电池放电时,负极的电极反应式为,Li+向正极移动(填“正极”或“负极“).
②一种回收电极中Co元素的方法是:将LiCoO2与H2O2、H2SO4反应生成CoSO4.该反应的化学方程式为2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+4H2O+O2↑
(3)BASF高压法制备醋酸采用钴碘催化循环过程如图1所示,该循环的总反应方程式为CO+CH3OH→CH3COOH(反应条件无需列出)
(4)某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx.不同温度下,将10mol模拟尾气(成分如图2所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如表
| 模拟尾气 | 气体 | 碳烟 | ||
| NO | O2 | He | ||
| 物质的量分数或物质的量 | 0.25% | 5% | 94.75% | a mol |
②实验过程中采用NO模拟NOx,而不采用NO2的原因是NO较NO2稳定,NO2气体中存在N2O4,不便于定量测定.
4.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 0.1mol•L-1NaOH溶液中通入SO2气体至pH=7:c(Na+)=c(HSO3-)+2 c(SO32-)+c(H2SO3) | |
| C. | 等物质的量浓度的CH3COOH溶液与NaOH溶液等体积混合后所得pH=9的溶液:c(OH-)-c(CH3COOH)=c(H+)=l×10-9mol•L-1 | |
| D. | 20 mL0.1mol•L-1CH3COONa溶液与10 mL 0.1mol•L-1HCl溶液混合得到的溶液:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) |
3.下列实验操作、现象与所得结论一致的是( )
0 161904 161912 161918 161922 161928 161930 161934 161940 161942 161948 161954 161958 161960 161964 161970 161972 161978 161982 161984 161988 161990 161994 161996 161998 161999 162000 162002 162003 162004 162006 162008 162012 162014 162018 162020 162024 162030 162032 162038 162042 162044 162048 162054 162060 162062 162068 162072 162074 162080 162084 162090 162098 203614
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向沸水中滴入几滴FeCl3饱和溶液,继续煮沸,并用激光笔照射 | 溶液变红褐色,出现 丁达尔效应 | 产生了 Fe(OH)3胶体 |
| B | 向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 | 溶液变蓝 | 氧化性:Fe3+>I2 |
| C | 将溴乙烷和NaOH的乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| D | 向滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液 | 溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
| A. | A | B. | B | C. | C | D. | D |

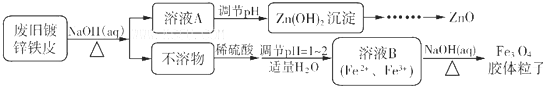
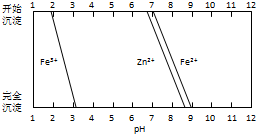 铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为: