题目内容
2.明矾石的主要成分是K2SO4•Al2(SO4)3•2Al2O3•6H2O,此外还含有少量Fe2O3杂质.利用明矾石制备氢氧化铝的流程如下: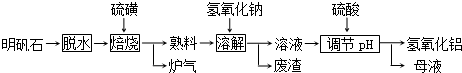
回答下列问题:
(1)“焙烧”过程中发生的反应为2Al2(SO4)3+3S $\frac{\underline{\;高温\;}}{\;}$ 2Al2O3+9SO2↑,其中氧化剂是Al2(SO4)3,若生成氧化铝0.5mol,则转移电子数目为3.
(2)“溶解”时反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
(3)“炉气”、“废渣”中的主要物质分别是SO2、Fe2O3.
(4)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是取最后一次洗涤的流出液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净.
(5)Al(OH)3可用于治疗胃酸过多,请写出相应的化学方程式Al(OH)3+6HCl=AlCl3+3H2O.
分析 明矾石制备氢氧化铝的流程:明矾石脱水后与硫磺焙烧,发生的反应为:2Al2(SO4)3+3S$\frac{\underline{\;高温\;}}{\;}$2Al2O3+9SO2↑,故生成炉气中含二氧化硫,熟料中含氧化铝、氧化铁、硫酸钾等,加入氢氧化钠和水,氧化铝和氢氧化钠反应生成偏铝酸钠,氧化铁不反应,过滤,滤渣中含氧化铁,滤液中含偏铝酸钠和硫酸钾、氢氧化钠等;用硫酸调节pH,得到氢氧化铝沉淀和硫酸钠、硫酸钾,过滤得母液中含硫酸钾、硫酸钠溶质,据此分析作答.
解答 解:(1)反应的化学方程式为2Al2(SO4)3+3S$\frac{\underline{\;高温\;}}{\;}$2Al2O3+9SO2↑,Al2(SO4)3化合价降低得电子为氧化剂,反应中失电子被氧化的S为3mol,故反应中转移电子数为:3×4=12mol,生成0.5mol Al2O3,则转移电子数为3mol;
故答案为:Al2(SO4)3;3;
(2)氢氧化钠与氧化铝反应生成偏铝酸钠和水,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O;
故答案为:Al2O3+2OH-=2AlO2-+H2O;
(3)由分析可知炉气中含二氧化硫,熟料中含氧化铝、氧化铁、硫酸钾等,加入氢氧化钠和水,氧化铝和氢氧化钠反应生成偏铝酸钠,氧化铁不反应,过滤,废渣中含氧化铁;
故答案为:SO2、Fe2O3;
(4)Al(OH)3沉淀具有吸附性,可吸附硫酸根离子,通过检验硫酸根离子的方法进行实验,方法为取最后一次洗涤的流出液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净;
故答案为:取最后一次洗涤的流出液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净;
(5)Al(OH)3与胃酸中的盐酸反应生成氯化铝和水,化学方程式为:Al(OH)3+6HCl=AlCl3+3H2O;
故答案为:Al(OH)3+6HCl=AlCl3+3H2O.
点评 本题考查了物质的制备,涉及对工艺流程的理解、氧化还原反应、对条件的控制选择与理解、等,理解工艺流程原理是解题的关键,是对学生综合能力的考查,需要学生具备扎实的基础与灵活运用能力,题目难度不大.

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案| A. | 共价化合物的熔沸点都比较低 | |
| B. | 氢的三种核素可组成6种水分子 | |
| C. | H2O分子比H2S分子稳定的原因,是H2O分子间存在氢键 | |
| D. | SiO2和CaCO3在高温下反应生成CO2气体,说明硅酸的酸性比碳酸强 |
| 苯甲醛 | 苯甲酸 | 苯甲醇 | |
| 沸点/℃ | 178.1 | 249.2 | 205.4 |
| 熔点/℃ | -26 | 121.7 | -15.3 |
| 溶解性 ( 常温 ) | 微溶于水,易溶于有机溶剂 | ||
| A. | 苯甲醛既发生了氧化反应,又发生了还原反应 | |
| B. | 可用银氨溶液判断反应是否完全 | |
| C. | 反应后的溶液先用分液法分离出有机层,再用蒸馏法分离出苯甲醇 | |
| D. | 反应后的溶液中加酸、酸化后,用过滤法分离出苯甲酸 |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向沸水中滴入几滴FeCl3饱和溶液,继续煮沸,并用激光笔照射 | 溶液变红褐色,出现 丁达尔效应 | 产生了 Fe(OH)3胶体 |
| B | 向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 | 溶液变蓝 | 氧化性:Fe3+>I2 |
| C | 将溴乙烷和NaOH的乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| D | 向滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液 | 溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
| A. | A | B. | B | C. | C | D. | D |
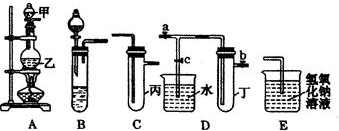
(1)将A、C、E相连后,以二氧化锰和浓盐酸(填写名称)为原料制取Cl2,仪器乙的名称是圆底烧瓶.
(2)利用(1)中装置和药品,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将所得氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 向所得氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生一种酸性强于碳酸的物质 |
实验Ⅱ获得结论是否合理?不合理(填“合理”或“不合理”).请写出产生气泡的离子方程式HCO3-+H+=CO2↑+H2O
(3)利用(1)中装置还可设计一个简单的实验比较Cl-和S2-的还原性强弱.若C中加入硫酸钾溶液,则C中预期出现的现象是产生淡黄色沉淀.
(4)将B、D、E装置相连接(打开止水夹a和止水夹b,关闭止水夹c),在B中盛装浓硝酸和铜片(将铜片放在有孔塑料板上),可制得NO2.一段时间后,欲用D装置探究NO2与水的反应,其操作步骤为:先关闭a、b,打开c再双手紧握(或微热)试管丁,使NO2逸出与水接触以使烧杯中的水进入试管丁,观察现象,E装置的作用是吸收尾气防止污染空气.
| A. | 等质量的NaOH和KOH分别与足量的盐酸反应,前者消耗HCl的量比后者少 | |
| B. | 观察钠元素焰色反应的颜色要透过蓝色钴玻璃进行观察 | |
| C. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为2CaO•5MgO•8SiO2•H2O |
| A. | 1L 1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 78g苯中含有C=C键的数目为3NA | |
| C. | 7.8gNa2O2固体中含有的离子总数为0.3NA | |
| D. | 标准状况下,将分子总数为NA的NO和O2充分混合后,所得混合气体的体积约为22.4L |
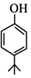 ,同时满足下列条件的X的同分异构体共有26种.(①苯环上有三个取代基 ②能与FeCl3溶液显色)写出其中苯环上只有两种不同化学环境氢原子的两种异构体的结构简式:
,同时满足下列条件的X的同分异构体共有26种.(①苯环上有三个取代基 ②能与FeCl3溶液显色)写出其中苯环上只有两种不同化学环境氢原子的两种异构体的结构简式: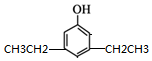 、
、 .
.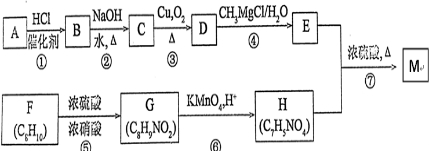
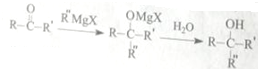
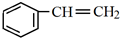 ,H中官能团的名称为羧基、硝基.
,H中官能团的名称为羧基、硝基.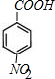 +
+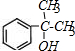 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O. 、
、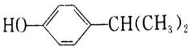 .(任写一种)
.(任写一种)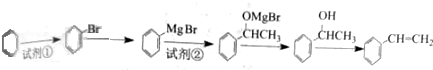
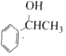 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$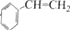 +H2O.
+H2O.