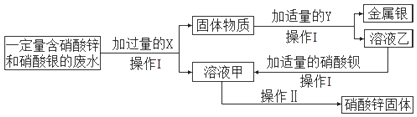
8.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
| A. | 常温下,48gO3和48gO2含有的电子数目为3NA | |
| B. | 1molOH-离子中含电子数目为10 NA | |
| C. | 0.5L0.2mol•L-1的NaCl溶液中含有的Na+数是0.1 NA | |
| D. | 33.6LCO中含有的原子总数是3NA |
7.1g O2和1g O3相比,下列表述正确的是( )
| A. | 所含分子数相同 | B. | 1g O3中所含分子数较多 | ||
| C. | 所含原子数不同 | D. | 所含原子数相同 |
6.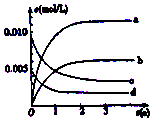 800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
 800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )
800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)?2NO2(g) n(NO)随时间的变化如表:( )| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO) (mol) | 0.020 | 0.010 | 0.009 | 0.008 | 0.008 | 0.008 |
| A. | a线表示NO2的变化趋势,则0~2s内v(NO2)=0.006mol/(L•s) | |
| B. | 800℃时,该反应的平衡常数K=1125L/mol | |
| C. | 能使该反应的反应速率增大,且平衡向正方向移动的措施是及时分理出NO2 | |
| D. | 已知:K300℃>K350℃,则该反应时吸热反应 |
5.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知H2(g)+Cl2(g)═2HCl(g)△H=-185kJ/mol,则氢气的燃烧热为185 kJ/mol | |
| B. | 已知石墨比金刚石稳定,则C (石墨,s)═C(金刚石,s)△H<0 | |
| C. | 已知2C(s)+2O2(g)═2CO2(g)△H1,2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 | |
| D. | 已知Ni(CO)4(s)═Ni(s)+4CO(g)△H=+Q kJ•mol-1,则Ni(s)+4CO(g)═Ni(CO)4(s)△H=-Q kJ•mol-1 |
3.下列说法正确的是( )
| A. | 乙烯的电子式为  | B. | 乙烯的球棍模型为 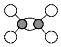 | ||
| C. | 乙烯分子是平面结构 | D. | 乙烯的结构简式为CH2CH2 |
2.下列关于烷烃性质的叙述中,不正确的是( )
| A. | 烷烃同系物随着相对分子质量增大,熔点、沸点逐渐升高 | |
| B. | 烷烃都能使溴水、酸性KMnO4溶液褪色 | |
| C. | 烷烃跟卤素单质在光照条件下能发生取代反应 | |
| D. | 烷烃同系物的密度随着相对分子质量的增大逐渐增大 |
1.下列事实不能说明亚硝酸( HNO2)是弱电解质的是( )
| A. | HNO2不跟NaCl反应 | |
| B. | NaNO2溶液的pH大于7 | |
| C. | 常温下0.lmol/L HNO2溶液的pH为2.145 | |
| D. | 相同温度下,用相同浓度的HCl溶液和HNO2溶液作导电试验,HNO2溶液灯泡较暗 |
20.在实验室中,对下来事故或药品的处理正确的是( )
| A. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| B. | 未使用完的白磷要随时收集起来,并与空气隔绝 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 含硫酸的废液倒入水槽,用水冲入下水道 |
19.下列金属冶炼的反应原理正确的是( )
0 161833 161841 161847 161851 161857 161859 161863 161869 161871 161877 161883 161887 161889 161893 161899 161901 161907 161911 161913 161917 161919 161923 161925 161927 161928 161929 161931 161932 161933 161935 161937 161941 161943 161947 161949 161953 161959 161961 161967 161971 161973 161977 161983 161989 161991 161997 162001 162003 162009 162013 162019 162027 203614
| A. | 2Al2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Al+3CO2↑ | B. | CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑ | ||
| C. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 | D. | 2HgO$\frac{\underline{\;电解\;}}{\;}$2Hg+O2↑ |