15.常温下,由水电离出C(H+)=1×10-13mol/L溶液中,一定能大量共存是( )
| A. | NH4+、Ba2+、Br-、CO32- | B. | K+、Na+、SO32-、MnO4- | ||
| C. | Al3+、Na+、AlO2-、Cl- | D. | Na+、Ba2+、Cl-、NO3- |
14.下列有关性质的比较不正确的是( )
| A. | 非金属性:Cl>Br | B. | 酸性:H2SO4>H3PO4 | ||
| C. | 碱性:KOH>NaOH | D. | 热稳定性:Na2CO3<NaHCO3 |
12.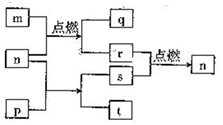 短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )
短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )
 短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )
短周期主感元素X、Y、Z、W原子序数依次增大,W2+的电子层结构与氖相同,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种碱性氧化物,它们的关系如图所示( )| A. | Y、Z、W的简单离子半径:W>Z>Y | B. | 最高价氧化物的水化物的碱性:Z>W | ||
| C. | 简单气态氢化物的热稳定性:X>Y | D. | Y与Z形成的化合物中不含有共价键 |
11.下列有关问题,与盐类的水解无关的是( )
| A. | NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 | |
| B. | 盐酸可作铁制品的除锈剂 | |
| C. | 实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 | |
| D. | 将FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |
10.下列物质在水溶液中的电离方程式错误的是( )
| A. | (NH4)2SO4=2NH4++SO42- | B. | NaHS?Na++HS${\;}^{_}$,HS-=H++S2- | ||
| C. | Ba(OH)2=Ba2++2OH- | D. | HF?H++F- |
9.下列说法正确的是( )
| A. | C8H10中只有3种属于芳香烃的同分异构体 | |
| B. | 苯与溴水混合振荡,水层颜色变浅 | |
| C. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| D. | 油脂、蛋白质、纤维素均属于高分子化合物,可以发生水解 |
7.(1)已知25℃时有关弱酸的电离平衡常数:
①等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为c b d a(填序号).
②25℃时,将20mL 0.1mol•L-1 CH3COOH溶液和20mL 0.1mol•L-1 HSCN溶液分别与20mL 0.1mol•L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图1所示: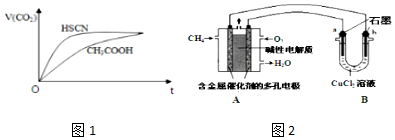
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快.
反应结束后所得两溶液中,c(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
③若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是b(填序号).
a.c(CH3COO-)b.c(H+)c.Kw d.醋酸电离平衡常数
(2)甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.一定条件下,用甲烷可以消除氮氧化物(NOx)的污染.已知:
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H1
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8kJ热量.
①该混合气体中NO和NO2的物质的量之比为3:1
②已知上述热化学方程式中△H1=-1160kJmol,则△H2=-574 kJ/mol.
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式4NO(g)=2NO2(g)+N2(g)△H=-293KJ/mol
(3)甲烷燃料电池可以提升能量利用率.图2是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
请回答:
①甲烷燃料电池的负极反应式是CH4-8e-+10OH-=CO32-+7H2O
②当A中消耗0.15mol氧气时,B中b极增重6.4g.
0 161763 161771 161777 161781 161787 161789 161793 161799 161801 161807 161813 161817 161819 161823 161829 161831 161837 161841 161843 161847 161849 161853 161855 161857 161858 161859 161861 161862 161863 161865 161867 161871 161873 161877 161879 161883 161889 161891 161897 161901 161903 161907 161913 161919 161921 161927 161931 161933 161939 161943 161949 161957 203614
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7K2=5.6×10-11 |
②25℃时,将20mL 0.1mol•L-1 CH3COOH溶液和20mL 0.1mol•L-1 HSCN溶液分别与20mL 0.1mol•L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图1所示:

反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快.
反应结束后所得两溶液中,c(CH3COO-)<c(SCN-)(填“>”、“<”或“=”)
③若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是b(填序号).
a.c(CH3COO-)b.c(H+)c.Kw d.醋酸电离平衡常数
(2)甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.一定条件下,用甲烷可以消除氮氧化物(NOx)的污染.已知:
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H1
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8kJ热量.
①该混合气体中NO和NO2的物质的量之比为3:1
②已知上述热化学方程式中△H1=-1160kJmol,则△H2=-574 kJ/mol.
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式4NO(g)=2NO2(g)+N2(g)△H=-293KJ/mol
(3)甲烷燃料电池可以提升能量利用率.图2是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
请回答:
①甲烷燃料电池的负极反应式是CH4-8e-+10OH-=CO32-+7H2O
②当A中消耗0.15mol氧气时,B中b极增重6.4g.
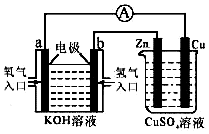 由化学能转变的热能或电能仍然是人类使用的主要能源,根据如图所示的装置,(其中a、b均为石墨电极)
由化学能转变的热能或电能仍然是人类使用的主要能源,根据如图所示的装置,(其中a、b均为石墨电极)