15.煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.已知反应CO(g)+H2O(g)?CO2(g)+H2(g)在恒容容器中进行,平衡常数随温度的变化如表:下列判断正确的是( )
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| A. | 达平衡后升温,反应速率增大,压强减小 | |
| B. | 其他条件不变,增加压强能提高CO的转化率 | |
| C. | 该反应△H>0 | |
| D. | 830℃时,在2 L的密闭容器中加入4 mol CO(g)和4 mol H2O(g),平衡时,CO的转化率是50% |
14.已知下列反应:CO(g)+2H2(g)═CH3OH(g)△H1①;2H2(g)+O2(g)═2H2O(l)△H2 ②;2CO(g)+O2(g)═2CO2(g)△H3③;2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l)△H4④.下列关系正确的是( )
| A. | △H4=△H3+△H2+△H1 | B. | △H4=△H3+2△H2+2△H1 | ||
| C. | △H4=△H3+2△H2-2△H1 | D. | △H4=△H3+2△H2-△H1 |
13.下列有关溶液中离子存在和转化表述不正确的是( )
| A. | 常温下,水电离出的c(H+)=1×10-12 mol/L的溶液中不可能大量存在:Al3+、NH4+、Cl-、S2- | |
| B. | 加入铝粉能产生H2的溶液中可能大量存在:Na+、Cl-、S2-、SO32- | |
| C. | 过量铁粉与稀HNO3反应:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | 向AlCl3溶液中滴入大量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
12.下列关于反应与能量的说法正确的是( )
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216 kJ/mol:E反应物<E生成物 | |
| B. | CaCO3(s)═CaO(s)+CO2(g)△H=+178.2 kJ/mol:E反应物<E生成物 | |
| C. | HCl(g)═$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)△H=+92.3 kJ/mol:1 mol HCl在密闭容器中分解后放出92.3 kJ的热量 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol:含1 mol NaOH的烧碱溶液与含0.5 mol H2SO4的浓H2SO4混合后放出57.3 kJ的热量 |
11.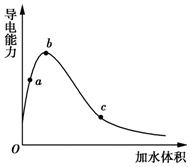 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )| A. | a、b、c三点溶液的pH:c<a<b | |
| B. | 用湿润的pH试纸测量a处溶液的pH,测量结果偏小 | |
| C. | a、b、c三点CH3COOH的电离程度:c<a<b | |
| D. | a、b、c三点溶液用1 mol•L-1 NaOH溶液中和,消耗NaOH溶液体积:c<a<b |
10.下列热化学方程式正确的是( )
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)$?_{催化剂}^{500℃、30M}$2NH3(g)?△H=-38.6 kJ•mol-1 | |
| C. | S(s)+O2(g)═SO2(g)△H=-269.8 kJ•mol-1 | |
| D. | 2NO2═O2+2NO△H=+116.2 kJ•mol-1 |
9.关于如图所示的过程,下列说法不正确的是( )
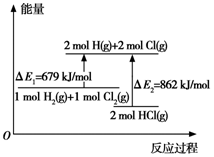

| A. | △E1是该反应的活化能 | B. | △E2是2 mol H-Cl键的总键能 | ||
| C. | 加入催化剂可以改变反应的焓变 | D. | 该反应是一个放热反应 |
8.反应A(g)+3B(g)═2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.25mol/(L•s),
②v(B)=27mol/(L•min),
③v(C)=0.4mol/(L•s),
④v(D)=36mol/(L•min).
下列有关反应速率的比较中正确的是( )
①v(A)=0.25mol/(L•s),
②v(B)=27mol/(L•min),
③v(C)=0.4mol/(L•s),
④v(D)=36mol/(L•min).
下列有关反应速率的比较中正确的是( )
| A. | ④>②>③>① | B. | ①>④>②>③ | C. | ①>②>③>④ | D. | ④>①>③>② |
7.下列实验不能达到实验目的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 测定相同物质的量浓度的KOH和氨水的pH | 证明氨水中存在电离平衡 |
| B | 向混有NaCl的NaOH溶液中滴入已知浓度的盐酸(用酚酞作指示剂) | 滴定其中NaOH含量 |
| C | 将Mg、Al和NaOH溶液设计为原电池 | 比较Mg、Al活泼性强弱 |
| D | 用惰性电极电解饱和食盐水,阴极附近滴加酚酞 | 验证阴极有碱生成 |
| A. | A | B. | B | C. | C | D. | D |
6.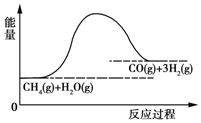 合成氨用的H2可以CH4为原料制得:CH4(g)+H2O(g)═CO(g)+3H2(g).反应过程的能量变化如图所示,关于该反应的下列说法中,正确的是( )
合成氨用的H2可以CH4为原料制得:CH4(g)+H2O(g)═CO(g)+3H2(g).反应过程的能量变化如图所示,关于该反应的下列说法中,正确的是( )
0 161751 161759 161765 161769 161775 161777 161781 161787 161789 161795 161801 161805 161807 161811 161817 161819 161825 161829 161831 161835 161837 161841 161843 161845 161846 161847 161849 161850 161851 161853 161855 161859 161861 161865 161867 161871 161877 161879 161885 161889 161891 161895 161901 161907 161909 161915 161919 161921 161927 161931 161937 161945 203614
 合成氨用的H2可以CH4为原料制得:CH4(g)+H2O(g)═CO(g)+3H2(g).反应过程的能量变化如图所示,关于该反应的下列说法中,正确的是( )
合成氨用的H2可以CH4为原料制得:CH4(g)+H2O(g)═CO(g)+3H2(g).反应过程的能量变化如图所示,关于该反应的下列说法中,正确的是( )| A. | △H<0,△S<0 | B. | △H>0,△S<0 | C. | △H<0,△S>0 | D. | △H>0,△S>0 |