2.下列根据实验操作和现象所得出的结论不正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中不一定含有SO42- |
| B | FeCl2溶液中,滴加KSCN溶液和溴水 | 滴加KSCN溶液,无明显变化;滴加溴水后,溶液变为血红色 | 氧化性:Br2>Fe3+ |
| C | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| D | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |
| A. | A | B. | B | C. | C | D. | D |
1.用下列装置进行相应实脸,不能达到实验目的是( )
| A. |  如图装置可用于制备氢氧化亚铁 | |
| B. | 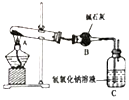 如图装置可用于测定Na2CO3和NaHCO3混合物中NaHCO3的含量 | |
| C. |  如图装置可用于检验氨气溶于水后显碱性 | |
| D. |  如图装置可用于CaCO3和稀盐酸反应制取少量的CO2气体 |
19.X、Y、Z、W、V均为短周期元素,且Y、Z、W、V在周期表的位置关系如表.已知X与W能形成最简单的有机物,则下列有关说法正确的是( )
| W | |||
| Y | Z | V |
| A. | W有多种同素异形体,且均具有高熔点、高沸点的性质 | |
| B. | Z的第一电离能小于V的第一电离能 | |
| C. | Y、Z与X的常见稳定液态氧化物反应的剧烈程度Y大于Z | |
| D. | X的离子半径一定小于与Y同族的短周期元素的离子半径 |
18.下列条件一定能使反应速率增大的有几项( )
①增加反应物的物质的量
②升高温度
③缩小反应容器的体积
④不断分离出生成物.
①增加反应物的物质的量
②升高温度
③缩小反应容器的体积
④不断分离出生成物.
| A. | 4项 | B. | 3项 | C. | 2项 | D. | 1项 |
17.下列离子组在室温下可能大量共存的是( )
| A. | pH=1的溶液:HCO3-、Na+、ClO-、NO3- | |
| B. | 无色溶液中可能大量存在:Al3+、NH4+、Cl-、S2- | |
| C. | 水电离出的c(H+)=10-4 mol/L的溶液:Na+、K+、SO42-、CO32- | |
| D. | 使石蕊呈红色的溶液:NH4+、NO3-、AlO2-、I- |
16.分类是学习和研究化学的一种重要方法,下列分类合理的是( )
| A. | K2CO3和K2O都属于钾盐 | B. | H2SO4和HNO3都属于酸 | ||
| C. | KOH和Na2CO3都属于碱 | D. | Na2O和Na2CO3都属于氧化物 |
15.下列反应中,SO2作为氧化剂而发生反应的是( )
| A. | 2SO2+O2═2SO3 | B. | SO2+H2O═H2SO3 | ||
| C. | SO2+2H2S═3S↓+2H2O | D. | SO2+Cl2+2H2O═H2SO4+2HCl |
14.证明某溶液含有Fe2+的实验方法是( )
| A. | 先滴加氯水,再滴加KSCN溶液后显红色 | |
| B. | 先滴加KSCN溶液,不显红色,再滴加氯水后显红色 | |
| C. | 滴加NaOH溶液,产生白色沉淀 | |
| D. | 只需滴加KSCN溶液 |
13.下列关于物质的性质或制备说法正确的是( )
0 161696 161704 161710 161714 161720 161722 161726 161732 161734 161740 161746 161750 161752 161756 161762 161764 161770 161774 161776 161780 161782 161786 161788 161790 161791 161792 161794 161795 161796 161798 161800 161804 161806 161810 161812 161816 161822 161824 161830 161834 161836 161840 161846 161852 161854 161860 161864 161866 161872 161876 161882 161890 203614
| A. | 用平行光照射氯化钠溶液和氢氧化铁胶体,产生的现象相同 | |
| B. | 铝具有较强的抗腐蚀性质,是因为铝与氧气常温下不反应 | |
| C. | 实验室用MnO2和稀盐酸反应制取氯气 | |
| D. | 工业上用电解熔融氧化铝制取金属铝 |