15.25℃时,下列有关溶液的说法正确的是( )
| A. | 往0.3mol/L的NH3•H2O溶液中加入少量NaOH固体,NH3•H2O的电离平衡向逆反应方向移动,同时溶液中c(OH-)•c(NH4+)/c(NH3•H2O)将减小 | |
| B. | PH=9的NaOH溶液和NH3•H2O溶液中,由水电离出的c(H+)前者小于后者 | |
| C. | 浓度均为0.1mol/L的CH3COOH与CH3COONa溶液等体积混合后,PH=5,则混合溶液中:c(CH3COO-)-c(CH3COOH)=2×(10-5-10-9)mol/L | |
| D. | 相同条件下,将足量的氢氧化铁固体加入到相同体积的下列溶液:①蒸馏水②0.1mol/L氢氧化钠③0.1mol/L氢氧化钡④0.1mol/L氯化铁,则铁离子浓度:④>①>②═③ |
10.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1mol甲基中含有电子数为10NA | |
| B. | 常温下,1LpH=12的Na2CO3溶液中含有的OH-离子数为0.01 NA | |
| C. | 标准状况下,NO和O2各11.2L混合充分反应,所得气体的分子总数为0.75 NA | |
| D. | 50mL12mol•L-1盐酸和足量MnO2共热,转移的电子数为0.3 NA |
9.如图为用含少量铁的废铜渣为原料生产胆矾的流程:

金属离子沉淀的pH
(1)写出浸出时铜与稀硝酸反应的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(2)在浸出时加入稀硫酸的作用提供酸性环境,使NO3-氧化铜
(3)试剂b为CuO或Cu(OH)2;滤渣c为Fe(OH)3.
(4)取样检验是为了证明没有Fe3+存在,其方法是向试样中滴加KSCN溶液,无明显现象.
(5)从滤液中得到胆矾的操作是蒸发浓缩、冷却结晶、过滤
(6)气体 a 可以被循环利用,用化学方程式表示气体 a 被循环利用的原理为2NO+O2=2NO2、3NO2+H2O=2HNO3+NO.
(7)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和 O2气体,且n (SO3):n (SO2)=1:2,写出硫酸铜受热分解的化学方程式3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑.

金属离子沉淀的pH
| 离子种类 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
(2)在浸出时加入稀硫酸的作用提供酸性环境,使NO3-氧化铜
(3)试剂b为CuO或Cu(OH)2;滤渣c为Fe(OH)3.
(4)取样检验是为了证明没有Fe3+存在,其方法是向试样中滴加KSCN溶液,无明显现象.
(5)从滤液中得到胆矾的操作是蒸发浓缩、冷却结晶、过滤
(6)气体 a 可以被循环利用,用化学方程式表示气体 a 被循环利用的原理为2NO+O2=2NO2、3NO2+H2O=2HNO3+NO.
(7)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和 O2气体,且n (SO3):n (SO2)=1:2,写出硫酸铜受热分解的化学方程式3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑.
7.下列离子方程式正确的是( )
0 161526 161534 161540 161544 161550 161552 161556 161562 161564 161570 161576 161580 161582 161586 161592 161594 161600 161604 161606 161610 161612 161616 161618 161620 161621 161622 161624 161625 161626 161628 161630 161634 161636 161640 161642 161646 161652 161654 161660 161664 161666 161670 161676 161682 161684 161690 161694 161696 161702 161706 161712 161720 203614
| A. | 向Fe2(SO4)3溶液中加入铁粉:Fe3++Fe═2Fe3+ | |
| B. | 石灰石溶于醋酸:CaCO3+2CH3COOH═2CH3COO-+Ca2++CO2↑+H2O | |
| C. | 铜跟浓硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ |
 .
.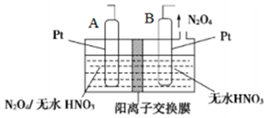 氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛.
氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛.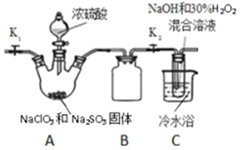 亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂.通常情况下,ClO2是一种具有强氧化性的黄色气体,常用于水的净化和纸浆、纺织品的漂白.ClO2易发生爆炸,在生产、使用时可用其它气体进行稀释.ClO2易与碱反应生成亚氯酸盐和氯酸盐.
亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂.通常情况下,ClO2是一种具有强氧化性的黄色气体,常用于水的净化和纸浆、纺织品的漂白.ClO2易发生爆炸,在生产、使用时可用其它气体进行稀释.ClO2易与碱反应生成亚氯酸盐和氯酸盐.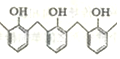 …的高聚物,其单体是甲醛和苯酚
…的高聚物,其单体是甲醛和苯酚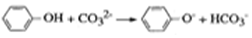
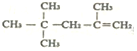 的名称为:2,4,4,-三甲基-1-戊烯
的名称为:2,4,4,-三甲基-1-戊烯