5.向22.4gFe2O3、Cu的混合物中加入0.5mol/L的硫酸溶液600mL,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,则固体剩余的质量为( )
| A. | 6.4g | B. | 4.8g | C. | 17.6g | D. | 20.2g |
4.下列有关物质的性质和用途的说法正确的是( )
| A. | 一定条件下,用秸秆可制得葡萄糖和酒精 | |
| B. | 铁制品表面涂“银粉”(铝粉)防生锈,是由于铝的化学性质比铁的稳定 | |
| C. | 氧气被用作火箭的燃料,利用了氧气的可燃性 | |
| D. | 稀有气体充入霓虹灯,利用了稀有气体通电时发出不同颜色的光的化学性质 |
2.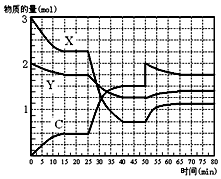 如图表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.下表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).
如图表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.下表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).
①X、Y、C三种气体发生反应的化学方程式为Y+3X?2C.
②表中a的取值范围是25.1<a<64.2.
③根据上图和上表分析,25min~40min内图中曲线发生变化的原因可能是缩小容器体积或增大压强.
 如图表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.下表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).
如图表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.下表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).| 压强/Mpa C% 温度/℃ | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.5 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
②表中a的取值范围是25.1<a<64.2.
③根据上图和上表分析,25min~40min内图中曲线发生变化的原因可能是缩小容器体积或增大压强.
1.检验某溶液中是否含有Cl-,正确的操作是( )
| A. | 取样,滴加AgNO3溶液,看是否有白色沉淀生成 | |
| B. | 取样,先加盐酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成 | |
| C. | 取样,加少量AgNO3溶液,有白色沉淀;再加稀硝酸,看白色沉淀是否消失 | |
| D. | 取样,先加稀硫酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成 |
20.检验某溶液中是否含有Cl-,正确的操作是( )
| A. | 取样,加少量AgNO3溶液,有白色沉淀;再加稀硝酸,看白色沉淀是否消失 | |
| B. | 取样,先加盐酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成 | |
| C. | 取样,先加稀硫酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成 | |
| D. | 取样,滴加AgNO3溶液,看是否有白色沉淀生成 |
19.室温下pH值相同的下列溶液中,浓度最大的是( )
| A. | Na2CO3 | B. | NaHCO3 | C. | NaOH | D. | CH3COONa |
18.为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g样品加热,其质量变为w2g,则该样品的纯度(质量分数)是( )
| A. | $\frac{84{w}_{2}-53{w}_{1}}{31{w}_{1}}$ | B. | $\frac{84{w}_{2}-53{w}_{1}}{31{w}_{1}}$ | ||
| C. | $\frac{84{w}_{2}-53{w}_{1}}{31{w}_{1}}$ | D. | $\frac{115{w}_{2}-84{w}_{1}}{31{w}_{1}}$ |
17.已知:SO32-+I2+H2O═SO42-+2I-+2H+.某溶液中可能含有 Na+、NH4+、Fe2+、K+、I-、SO32-、SO42-,且所有离子物质的量浓度相等.向该无色溶液中滴加少量溴水,溶液仍呈无色.下列关于该溶液的判断正确的是( )
0 161506 161514 161520 161524 161530 161532 161536 161542 161544 161550 161556 161560 161562 161566 161572 161574 161580 161584 161586 161590 161592 161596 161598 161600 161601 161602 161604 161605 161606 161608 161610 161614 161616 161620 161622 161626 161632 161634 161640 161644 161646 161650 161656 161662 161664 161670 161674 161676 161682 161686 161692 161700 203614
| A. | 肯定不含 I- | B. | 肯定不含 SO42- | C. | 可能含有 SO32- | D. | 肯定含有 NH4+ |