题目内容
5.向22.4gFe2O3、Cu的混合物中加入0.5mol/L的硫酸溶液600mL,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,则固体剩余的质量为( )| A. | 6.4g | B. | 4.8g | C. | 17.6g | D. | 20.2g |
分析 由2Fe3++Cu═2Fe2++Cu2+和“所得溶液中不含Fe3+”可知,Fe2O3的物质的量与铜的物质的量相等,设出物质的量为x,然后根据氧化铁和铜的质量列式计算二者的物质的量,再根据用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为氧化铁中氧元素质量,以此计算.
解答 解:由2Fe3++Cu═2Fe2++Cu2+和“所得溶液中不含Fe3+”可知,Fe2O3的物质的量与铜的物质的量相等,
设二者的物质的量都为xmol,则有160x+64x=22.4g,解得x=0.1mol,
用一氧化碳还原时,固体质量损失的是氧化铁中O的质量,0.1mol氧化铁中含有0.3molO,
则固体减少质量为m(O)=0.3mol×16g/mol=4.8g,
剩余固体为Fe、Cu,其质量为22.4g-4.8g=17.6g,
故选C.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应及物质的量关系为解答的关键,侧重分析与计算能力的考查,注意剩余固体为Fe、Cu的混合物,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)?N2O5(g)+O2(g).若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是( )
| A | B | C | D |
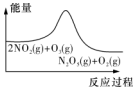 |  |  |  |
| 平衡后升温,NO2含量降低 | 0~2s内,v(O2)=0.2mol•L-1•s-1 | v正:b点>a点,b点:v逆>v正 | 恒温,t1时再充入O3 |
| A. | .A. | B. | .B | C. | .C | D. | .D |
4.加热28.6g石碱晶体(Na2CO3 •10H2O )后得到12.4g固体残渣,则残渣的化学式是( )
| A. | Na2CO3 •H2O | B. | Na2CO3 •2H2O | C. | Na2CO3 | D. | 无法计算 |
13.稀土元素是周期表中ⅢB族钪、钇和镧系元素之总称,金属活泼性仅次于碱金属和碱土金属元素,它们的性质极为相似,常见化合价为+3价.其中钇(Y)元素是激光和超导的重要材料.我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇.
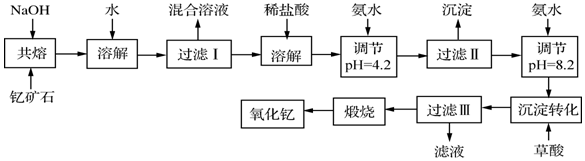
已知:
①有关金属离子形成氢氧化物沉淀时的pH见下表.
②Be(OH)2+2NaOH═Na2BeO2+2H2O
请回答下列问题:
(1)若改用氧化物的形式表示Y2FeBe2Si2O10组成,则化学式为Y2O3•FeO•2BeO•2SiO2
(2)过滤Ⅲ所得滤液的溶质主要有NH4Cl、(NH4)2C2O4(填化学式)
(3)①欲从过滤I所得混合溶液中制得Be(OH)2沉淀,最好选用bd两种试剂,再通过必要的操作即可实现.
a.NaOH溶液 b.氨水 c.CO2 d.盐酸
②写出Na2BeO2与足量盐酸发生反应的离子方程式BeO22-+4H+=Be2++2H2O.
(4)能否用氨水直接将溶液的pH调节至8.2,不能(填能或不能),(若不能,请说明理由)第一步用氨水是为了使Fe3+转化为沉淀而除去.
(5)写出沉淀转化步骤中沉淀转化的化学方程式2Y(OH)3+3H2C2O4═Y2(C2O4)3+6H2O.

已知:
①有关金属离子形成氢氧化物沉淀时的pH见下表.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
请回答下列问题:
(1)若改用氧化物的形式表示Y2FeBe2Si2O10组成,则化学式为Y2O3•FeO•2BeO•2SiO2
(2)过滤Ⅲ所得滤液的溶质主要有NH4Cl、(NH4)2C2O4(填化学式)
(3)①欲从过滤I所得混合溶液中制得Be(OH)2沉淀,最好选用bd两种试剂,再通过必要的操作即可实现.
a.NaOH溶液 b.氨水 c.CO2 d.盐酸
②写出Na2BeO2与足量盐酸发生反应的离子方程式BeO22-+4H+=Be2++2H2O.
(4)能否用氨水直接将溶液的pH调节至8.2,不能(填能或不能),(若不能,请说明理由)第一步用氨水是为了使Fe3+转化为沉淀而除去.
(5)写出沉淀转化步骤中沉淀转化的化学方程式2Y(OH)3+3H2C2O4═Y2(C2O4)3+6H2O.
20.检验某溶液中是否含有Cl-,正确的操作是( )
| A. | 取样,加少量AgNO3溶液,有白色沉淀;再加稀硝酸,看白色沉淀是否消失 | |
| B. | 取样,先加盐酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成 | |
| C. | 取样,先加稀硫酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成 | |
| D. | 取样,滴加AgNO3溶液,看是否有白色沉淀生成 |
10.有关pH计算结果一定正确的是( )
| A. | 强酸pH=a,加水稀释到10n倍,则pH=a+n | |
| B. | 弱酸pH=a,加水稀释到10n倍,则pH<a+n(a+n<7) | |
| C. | 强碱pH=b,加水稀释到10n倍,则pH=b-n | |
| D. | 弱碱pH=b,加水稀释到10n倍,则pH=b-n(b-n>7) |
17.下列离子的检验方法、现象及结论均合理的是( )
| A. | 向某溶液中先滴加氯水,再滴加KSCN溶滚,溶液显血红色,说明原溶液中含有Fe3+ | |
| B. | 向某溶液中滴加过量氨水,先有白色沉淀产生,然后沉淀溶解,说明原溶液中含有Al3+ | |
| C. | 向某溶液中滴加Ca(OH)2溶液,得到白色沉淀,说明原溶液中含有CO32- | |
| D. | 向某溶液中滴加过量NaOH溶液,得到蓝色沉淀,说明原溶液中含有Cu2+ |
15.下列实验操作、现象和结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向Al2(SO4)3溶液中滴加过量氨水 | 溶液先浑浊后澄清 | Al(OH )3能溶于氨水 |
| B | 将浓硫酸滴在胆矾晶体上 | 蓝色晶体变白 | 浓硫酸具有脱水性 |
| C | 将新制的氯水滴在蓝色石蕊试纸上 | 试纸先变红后褪色 | Cl2有漂白性 |
| D | 向某晶体的水溶液中加入2滴FeSO4溶液 | 产生特征蓝色沉淀 | 该晶体中一定含有[F e(CN)6]3- |
| A. | A | B. | B | C. | C | D. | D |