9. 取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )
取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )
 取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )
取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )| A. | a点 | B. | b点 | C. | c点 | D. | d点 |
8.下列变化中,必须由给出的物质与某种氧化剂发生反应才可实现的是( )
| A. | NH3→NO | B. | Fe3+→Fe2+ | C. | Cl2→NaClO | D. | NO2→HNO3 |
7.要将溶液中的Al3+沉淀完全,则下列试剂中的最佳试剂是( )
| A. | NaOH溶液 | B. | 浓氨水 | C. | NaCl溶液 | D. | Na2SO4溶液 |
6.下列反应中,不属于氧化还原反应的是(反应条件未给出)( )
| A. | Zn+2HCl═ZnCl2+H2↑ | B. | 4NH3+5O2═4NO+6H2O | ||
| C. | 2HClO═2HCl+O2↑ | D. | Ca(OH)2+CO2═CaCO3↓+H2O |
4.下列离子方程式中,书写正确的是( )
| A. | 过氧化钠与水反应:2O22-+2H2O═4OH-+O2↑ | |
| B. | 氧化铝与盐酸:O2-+2H+═H2O | |
| C. | NaOH溶液与小苏打溶液反应:HCO3-+OH-═CO32-+H2O | |
| D. | 氯气通入水中:Cl2+H2O?2H++Cl-+ClO- |
3.下列有关物质的性质或应用正确的是( )
| A. | 钠与硫酸铜溶液反应会置换出红色的铜 | |
| B. | 常温下干燥氯气与铁不反应,可以用钢瓶储存液氯 | |
| C. | SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 | |
| D. | 普通玻璃的组成可用Na2O•CaO•6SiO2表示,是纯净物 |
2.氯化亚铜晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化.氯化铜、氯化亚铜是重要的化工原料,广泛地用作有机合成催化剂.实验室中以粗铜(含杂质Fe)为原料,一种制备铜的氯化物的流程如图.
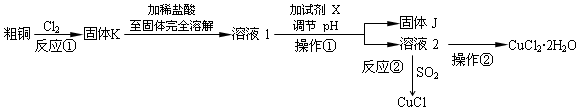
按要求回答下列问题:
(1)CuCl中Cu元素的化合价为+1价.操作②为加少量盐酸,蒸发浓缩、冷却结晶,过滤,洗涤,干燥
(2)溶液1可加试剂X用于调节pH,以除去杂质,试剂 X和固体J分别是c(填序号).
a.NaOH Fe(OH) b.NH3•H2O Fe(OH)2
c.CuO Fe(OH)3 d.CuSO4 Cu(OH)2
(3)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀.写出制备CuCl的离子方程式:2Cu2++2Cl-+SO2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+4H++SO42-.
(4)实验室保存新制CuCl晶体的方法是避光、密封保存.
(5)氯化亚铜的定量分析:
①称取样品0.250g和10mL过量的FeCl3溶液于250mL锥形瓶中,充分溶解.
②用0.100mol•L-1硫酸铈标准溶液滴定.
已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+.
三次平行实验结果如表(平行实验结果相差不能超过1%):
则样品中CuCl的纯度为95.5%(结果保留三位有效数字).
(6)如图所示将氯气从a通入与粗铜反应(铁架台、铁夹、酒精灯省略),
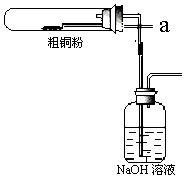
①反应时,盛粗铜粉的试管中的现象是产生大量棕黄色烟.
②反应后,盛有NaOH溶液的广口瓶中溶液具有漂白、消毒作用,若用钢铁(含Fe、C)制品盛装该溶液会发生电化学腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效.该电化学腐蚀过程中的正极反应式为ClO-+2e-+H2O=Cl-+2OH-.

按要求回答下列问题:
(1)CuCl中Cu元素的化合价为+1价.操作②为加少量盐酸,蒸发浓缩、冷却结晶,过滤,洗涤,干燥
(2)溶液1可加试剂X用于调节pH,以除去杂质,试剂 X和固体J分别是c(填序号).
a.NaOH Fe(OH) b.NH3•H2O Fe(OH)2
c.CuO Fe(OH)3 d.CuSO4 Cu(OH)2
(3)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀.写出制备CuCl的离子方程式:2Cu2++2Cl-+SO2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+4H++SO42-.
(4)实验室保存新制CuCl晶体的方法是避光、密封保存.
(5)氯化亚铜的定量分析:
①称取样品0.250g和10mL过量的FeCl3溶液于250mL锥形瓶中,充分溶解.
②用0.100mol•L-1硫酸铈标准溶液滴定.
已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+.
三次平行实验结果如表(平行实验结果相差不能超过1%):
| 平行次数 | 1 | 2 | 3 |
| 0.250g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
(6)如图所示将氯气从a通入与粗铜反应(铁架台、铁夹、酒精灯省略),

①反应时,盛粗铜粉的试管中的现象是产生大量棕黄色烟.
②反应后,盛有NaOH溶液的广口瓶中溶液具有漂白、消毒作用,若用钢铁(含Fe、C)制品盛装该溶液会发生电化学腐蚀,钢铁制品表面生成红褐色沉淀,溶液会失去漂白、杀菌消毒功效.该电化学腐蚀过程中的正极反应式为ClO-+2e-+H2O=Cl-+2OH-.
1.以下转化不能通过一步反应实现的是( )
| A. | Fe→FeCl3 | B. | SiO2→CaSiO3 | C. | Al2O3→Al(OH)3 | D. | Na2O2→NaOH |
20.下列试剂的保存或使用不正确的是( )
0 161436 161444 161450 161454 161460 161462 161466 161472 161474 161480 161486 161490 161492 161496 161502 161504 161510 161514 161516 161520 161522 161526 161528 161530 161531 161532 161534 161535 161536 161538 161540 161544 161546 161550 161552 161556 161562 161564 161570 161574 161576 161580 161586 161592 161594 161600 161604 161606 161612 161616 161622 161630 203614
| A. | 过氧化钠不可露置在空气中,要密封保存 | |
| B. | 剩余的金属钠应放回原试剂瓶 | |
| C. | 氢氟酸应密封保存在玻璃瓶中 | |
| D. | 实验室保存FeCl2时常向其中加入铁屑 |