题目内容
3.下列有关物质的性质或应用正确的是( )| A. | 钠与硫酸铜溶液反应会置换出红色的铜 | |
| B. | 常温下干燥氯气与铁不反应,可以用钢瓶储存液氯 | |
| C. | SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 | |
| D. | 普通玻璃的组成可用Na2O•CaO•6SiO2表示,是纯净物 |
分析 A.不符合反应客观事实;
B.氯气与铁反应需要在加热条件下;
C.二氧化硫不能漂白指示剂;
D.普通玻璃成分是:二氧化硅,硅酸钠和硅酸钙,比例根据原料比例不同而不同,为混合物.
解答 解:A.钠与硫酸铜溶液反应生成硫酸钠、氢气和氢氧化铜沉淀,故A错误;
B.常温下干燥氯气与铁不反应,可以用钢瓶储存液氯,故B正确;
C.SO2具有漂白性,但是不能是指示剂褪色,所以通入紫色石蕊溶液中能使溶液变红,故C错误;
D.普通玻璃成分是:二氧化硅,硅酸钠和硅酸钙,比例根据原料比例不同而不同,为混合物,故D错误;
故选:B.
点评 本题考查了元素化合物知识,明确相关物质的性质是解题关键,注意玻璃成分,注意钠与硫酸铜溶液反应实质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.在体积为V L的硫酸铝溶液中加入足量的氨水,过滤得沉淀,将沉淀洗净后灼烧至质量不再变化时冷却、称量,得mg白色固俸.原溶液中c(SO42-)为( )
| A. | $\frac{m}{V}$mol•L-1 | B. | $\frac{2m}{27V}$mol•L-1 | C. | $\frac{m}{18V}$mol•L-1 | D. | $\frac{m}{34V}$mol•L-1 |
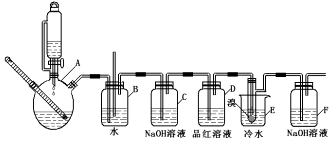
14.如图是实验室制备1,2-二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).
已知:
CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O
CH3CH2OH$→_{140℃}^{浓硫酸}$CH3CH2OCH2CH3+H2O
相关数据列表如表:
请完成下列填空:
(1)实验中应迅速将温度升高到170℃左右的原因是减少副产物乙醚生成.
(2)气体发生装置使用连通滴液漏斗的原因使连通滴液漏斗里的溶液容易滴下.
(3)安全瓶B在实验中有多重作用,其一可以检查实验进行中B后面的装置中导管是否发生堵塞,请写出发生堵塞时瓶B中的现象B中长直玻璃管内有一段液柱上升;
(4)装置D中品红溶液的作用是验证二氧化硫是否被除尽;
(5)容器C、F中都盛有NaOH溶液,F中NaOH溶液的作用是吸收挥发的溴蒸气;
(6)反应过程中用冷水冷却装置E不能过度冷却(如用冰水),其原因是过渡冷却1,2-二溴乙烷易凝结成固体而发生堵塞.
(7)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,如果装置的气密性没有问题,试分析可能的原因:①浓硫酸将部分乙醇氧化②发生副反应生成乙醚③乙醇挥发④乙烯流速过快,未完全发生加成反应;(写出两条即可)
(8)除去产物中少量未反应的Br2后,还含有的主要杂质为乙醚,要进一步提纯,下列操作中必须用到的是D(填入正确选项前的字母);
A.重结晶 B.过滤 C.萃取 D.蒸馏.

已知:
CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O
CH3CH2OH$→_{140℃}^{浓硫酸}$CH3CH2OCH2CH3+H2O
相关数据列表如表:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 | 3.10 |
| 沸点/℃ | 78.5 | 132 | 34.6 | 58.8 |
| 熔点/℃ | -l30 | 9 | -1l6 | -7.2 |
| 水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)实验中应迅速将温度升高到170℃左右的原因是减少副产物乙醚生成.
(2)气体发生装置使用连通滴液漏斗的原因使连通滴液漏斗里的溶液容易滴下.
(3)安全瓶B在实验中有多重作用,其一可以检查实验进行中B后面的装置中导管是否发生堵塞,请写出发生堵塞时瓶B中的现象B中长直玻璃管内有一段液柱上升;
(4)装置D中品红溶液的作用是验证二氧化硫是否被除尽;
(5)容器C、F中都盛有NaOH溶液,F中NaOH溶液的作用是吸收挥发的溴蒸气;
(6)反应过程中用冷水冷却装置E不能过度冷却(如用冰水),其原因是过渡冷却1,2-二溴乙烷易凝结成固体而发生堵塞.
(7)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,如果装置的气密性没有问题,试分析可能的原因:①浓硫酸将部分乙醇氧化②发生副反应生成乙醚③乙醇挥发④乙烯流速过快,未完全发生加成反应;(写出两条即可)
(8)除去产物中少量未反应的Br2后,还含有的主要杂质为乙醚,要进一步提纯,下列操作中必须用到的是D(填入正确选项前的字母);
A.重结晶 B.过滤 C.萃取 D.蒸馏.
18.将100mL 1.0mol/L AlCl3溶液取出10mL,与这10mL溶液中Cl-物质的量浓度相等的是( )
| A. | 30mL 1.0mol/L NaCl溶液 | B. | 10mL2.0mol/L FeCl3溶液 | ||
| C. | 50mL1.5mol/L MgCl2溶液 | D. | 100mL1.0mol/L HCl溶液 |
8.下列变化中,必须由给出的物质与某种氧化剂发生反应才可实现的是( )
| A. | NH3→NO | B. | Fe3+→Fe2+ | C. | Cl2→NaClO | D. | NO2→HNO3 |
15.在注射之前,需要进行皮肤敏感性试验,目前属于最重要的抗生素是( )
| A. | 青霉素 | B. | 阿司匹林 | C. | 麻黄碱 | D. | 碳酸钙 |
12. 电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液分别滴定10.00mL 浓度均为0.100mol•L-1的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液电导率如图所示.下列说法不正确的是( )
电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液分别滴定10.00mL 浓度均为0.100mol•L-1的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液电导率如图所示.下列说法不正确的是( )
 电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液分别滴定10.00mL 浓度均为0.100mol•L-1的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液电导率如图所示.下列说法不正确的是( )
电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液分别滴定10.00mL 浓度均为0.100mol•L-1的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液电导率如图所示.下列说法不正确的是( )| A. | 曲线①代表滴定CH3COOH溶液的曲线 | |
| B. | 在相同温度下,A、B、C 三点溶液中水电离的 c(H+):B<A=C | |
| C. | D点溶液中:c(Cl-)=2c(OH-)-2c(H+) | |
| D. | A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.05mol•L-1 |
13.下列说法不正确的是( )
| A. | 钠在空气中燃烧时,先熔化,再燃烧,发出黄色火焰,生成过氧化钠 | |
| B. | 铝是地壳里含量最多的金属元素,在常温下,铝不能与氧气反应 | |
| C. | 青铜是我国使用最早的合金,钢是用量最大、用途最广的合金 | |
| D. | 铁在潮湿的空气中生成的氧化物疏松多孔,不能保护内层金属 |
 ;
;
 ;
;