7.在一定温度和压强下,把装有NO和NO2的混合气体的试管倒立于水中,充分反应后,试管内气体的体积缩小为原气体体积的$\frac{1}{2}$,则原混合气体中NO和NO2的体积比为( )
| A. | 3:l | B. | 1:3 | C. | 2:3 | D. | 3:2 |
5.将足量的CO2不断通入NaOH、Ca(OH)2、NaAlO2的混合溶液中〔已知NaAlO2与CO2反应生成Al(OH)3〕,则生成沉淀的物质的量与通入CO2的体积的关系可表示为( )
| A. | 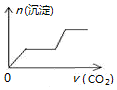 | B. | 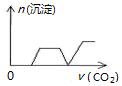 | C. | 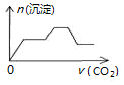 | D. |  |
4.常温下在下列溶液中加入足量的铁,充分反应后,生成气体最多的是( )
| A. | 20mL 12mol•L-1的盐酸 | B. | 10mL 18mol•L-1的硫酸 | ||
| C. | 80mL 2mol•L-1的硫酸 | D. | 40mL 14mol•L-1的硝酸 |
2.现有部分元素的性质与原子(或分子)结构如表:
(1)X形成的双原子分子的结构式为O=O,X形成的氢化物的沸点在同族元素形成的氢化物中是最高(填“最高”或“最低”),原因是水分子间存在氢键.
(2)金属冶炼Y单质的化学方程式为2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑.
(3)Y单质与W元素的最高价氧化物对应水化物恰好反应完全,向反应后的溶液中通入过量的CO2,发生反应的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-.
(4)单质Cu在一定条件下与足量Z元素形成的强酸浓溶液反应生成的气体是SO2(填化学式),检验该气体的常用试剂品红溶液.
| 元素编号 | 元素性质与原子(或分子)结构 |
| X | 地壳中含量最高的非金属元素 |
| Y | M层比K层多1个电子 |
| Z | 最外层电子数为内层电子数的0.6倍 |
| W | 与氯形成的氯化物是生活中常用的调味品 |
(2)金属冶炼Y单质的化学方程式为2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑.
(3)Y单质与W元素的最高价氧化物对应水化物恰好反应完全,向反应后的溶液中通入过量的CO2,发生反应的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-.
(4)单质Cu在一定条件下与足量Z元素形成的强酸浓溶液反应生成的气体是SO2(填化学式),检验该气体的常用试剂品红溶液.
5.在50mL18mol•L-1的浓H2SO4中加入足量的Cu片并加热,充分反应后,被还原的H2SO4的物质的量为( )
| A. | 等于0.9mol | B. | 等于0.45mol | ||
| C. | 大于0.45mol,小于0.9mol | D. | 小于0.45mol |
4.若在加入铝粉能产生氢气的无色溶液中,分别加入下列各组离子,可能共存的是( )
0 161339 161347 161353 161357 161363 161365 161369 161375 161377 161383 161389 161393 161395 161399 161405 161407 161413 161417 161419 161423 161425 161429 161431 161433 161434 161435 161437 161438 161439 161441 161443 161447 161449 161453 161455 161459 161465 161467 161473 161477 161479 161483 161489 161495 161497 161503 161507 161509 161515 161519 161525 161533 203614
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、AlO2-、K+、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | AlO2-、K+、NO3-、OH- |
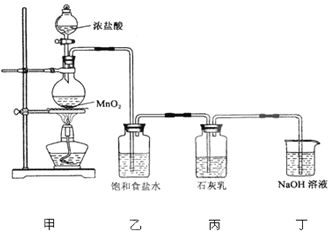
 ,Q3Y2与水可剧烈反应,反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3↑
,Q3Y2与水可剧烈反应,反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3↑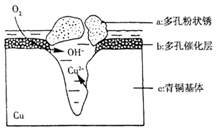 如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图.
如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图.