13.常温下,对于①0.1mol•L-1CH3COONa溶液,②pH=13的NaOH溶液,③pH=1的HC1溶液,
④0.1mol•L-1CH3COOH溶液,[已知Ka(CH3COOH)=1.75×10-5]下列说法正确的是( )
④0.1mol•L-1CH3COOH溶液,[已知Ka(CH3COOH)=1.75×10-5]下列说法正确的是( )
| A. | 水电离出的c(OH-):①>②>④>③ | |
| B. | ①和③混合后溶液呈中性:c(Na+)+c(H+)>c(CH3COO-)+c(Cl-) | |
| C. | ①和④混合后溶液呈酸性:$\frac{c(N{a}^{+})}{c(C{H}_{3}CO{O}^{-})}$=1 | |
| D. | ③和④分别稀释100倍后的pH④<③ |
12.对下列反应:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O判断合理的是( )
| A. | Fe(NO3)x中的x为3 | |
| B. | 标准状况下产生4.48LNO,就有0.5 mol电子转移 | |
| C. | 稀HNO3在反应中只作氧化剂 | |
| D. | 磁性氧化铁中的铁元素全部被氧化 |
11.下列各种操作中.不会导致液体分散系颜色发生两次显著变化的是( )
| A. | 向Fe(OH)3胶体中加入4 mol/LH2SO4至过量 | |
| B. | 向紫色石蕊试剂中通入过量C12 | |
| C. | 向紫色石蕊试剂中通入过量SO2 | |
| D. | 向酚酞试液中加入Na2O2粉末至过量 |
10.向盛有Cl2的六个集气瓶甲、乙、丙、丁、戊、己中各注入下列液体中的一种,经过振荡,现象如图所示,则甲、乙、丙、丁、戊、己注入的液体分别是( )
①AgNO3溶液 ②NaOH溶液 ③水 ④淀粉-KI溶液 ⑤FeCl2与KSCN混合液 ⑥NaBr溶液

①AgNO3溶液 ②NaOH溶液 ③水 ④淀粉-KI溶液 ⑤FeCl2与KSCN混合液 ⑥NaBr溶液

| A. | ④①②⑥⑤③ | B. | ⑥①③④②⑤ | C. | ⑥③②④①⑤ | D. | ②①③④⑥⑤ |
8.2.0g NaOH固体溶于水配成100mL溶液,溶液中C(Na+)为( )
| A. | 0.2 mol/L | B. | 0.3mol/L | C. | 0.4 mol/L | D. | 0.5 mol/L |
7.若20g密度为ρ g•cm-3的Ca(NO3)2(相对分子质量为164)溶液中含有1g Ca(NO3)2,则溶液中NO3-的物质的量浓度为( )
| A. | $\frac{100ρ}{41}$ mol•L-1 | B. | $\frac{20}{ρ}$ mol•L-1 | C. | $\frac{50ρ}{41}$ mol•L-1 | D. | $\frac{25ρ}{41}$ mol•L-1 |
6.有关实验操作,下列说法中正确的是( )


| A. | 甲装置可用于灼烧胆矾,制备无水硫酸铜 | |
| B. | 乙装置可用于分离溴单质与四氯化碳 | |
| C. | 丙装置可用于蒸馏,分离乙醇和水 | |
| D. | 丁装置可用于过滤,分离汽油和水的混合物 |
5.某无色溶液中可能存在如下几种阴阳离子:
现对该溶液样品进行以下研究:
Ⅰ.向溶液中加入稀盐酸后有无色气体生成,该气体遇空气变成红棕色;
Ⅱ.若向Ⅰ所得溶液中加入BaCl2溶液,有白色沉淀生成;
Ⅲ.若向Ⅰ所得溶液中加入过量NaOH浓溶液并加热,产生有刺激性气味的气体,最终溶液无沉淀生成;
Ⅳ.向Ⅲ所得溶液中通入过量的CO2气体,有白色絮状沉淀生成.
根据上述实验,回答下列问题:
(1)该溶液中一定存在的阳离子为Al3+、NH4+,一定不存在的离子为Fe2+、Ba2+、CO32-.
(2)检验溶液中可能还存在的阳离子的方法为用洁净铂丝蘸取原溶液进行焰色反应,若火焰呈黄色,原溶液中存在Na+,若不出现黄色,则不存在Na+.
(3)写出实验Ⅰ发生反应的离子方程式:6I-+2NO3-+8H+=2NO↑+3I2+4H2O.
(4)写出实验Ⅳ中生成白色絮状沉淀的化学方程式:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3.
0 161273 161281 161287 161291 161297 161299 161303 161309 161311 161317 161323 161327 161329 161333 161339 161341 161347 161351 161353 161357 161359 161363 161365 161367 161368 161369 161371 161372 161373 161375 161377 161381 161383 161387 161389 161393 161399 161401 161407 161411 161413 161417 161423 161429 161431 161437 161441 161443 161449 161453 161459 161467 203614
| 阳离子 | Al3+、Fe2+、Ba2+、Na+、NH4+ |
| 阴离子 | Cl-、CO32-、SO42-、NO3-、I- |
Ⅰ.向溶液中加入稀盐酸后有无色气体生成,该气体遇空气变成红棕色;
Ⅱ.若向Ⅰ所得溶液中加入BaCl2溶液,有白色沉淀生成;
Ⅲ.若向Ⅰ所得溶液中加入过量NaOH浓溶液并加热,产生有刺激性气味的气体,最终溶液无沉淀生成;
Ⅳ.向Ⅲ所得溶液中通入过量的CO2气体,有白色絮状沉淀生成.
根据上述实验,回答下列问题:
(1)该溶液中一定存在的阳离子为Al3+、NH4+,一定不存在的离子为Fe2+、Ba2+、CO32-.
(2)检验溶液中可能还存在的阳离子的方法为用洁净铂丝蘸取原溶液进行焰色反应,若火焰呈黄色,原溶液中存在Na+,若不出现黄色,则不存在Na+.
(3)写出实验Ⅰ发生反应的离子方程式:6I-+2NO3-+8H+=2NO↑+3I2+4H2O.
(4)写出实验Ⅳ中生成白色絮状沉淀的化学方程式:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3.
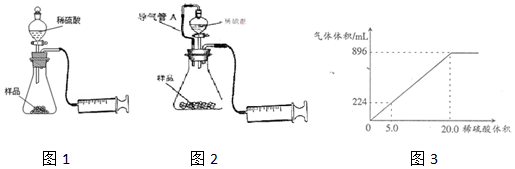
 .
.