题目内容
14.某学校化学兴趣小组从文献资料上获得如下信息:NaHCO3在潮湿的空气中会缓慢分解成Na2CO3、H2O和CO2.为了验证这一信息,该科研小组将一瓶在潮湿空气中久置的NaHCO3样品混合均匀后,进行如下探究: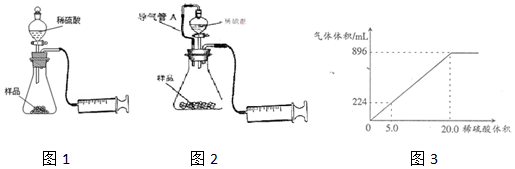
【探究目的】实验测定样品中NaHCO3、Na2CO3的物质的量之比
【探究思路】设计实验测量有关反应物和生成物的量,并通过计算确定样品中NaHCO3、Na2CO3的物质的量之比
【实验探究】
方案甲:实验装置如图1所示.将一定质量的混合物样品加入锥形瓶中,通过分液漏斗加入一定体积的稀硫酸充分反应,在用针筒收集并确定生成气体体积(忽略针筒管壁间的摩擦).
(1)充分反应后,针筒中气体读数为V mL,则反应中生成的CO2气体体积>V mL(填“=、<或>”).
(2)有同学对实验测量结果提出异议,认为图1装置会导致较大的实验误差,应该用图2装置,则导气管A的作用是平衡分液漏斗内和锥形瓶中气体压强,使得溶液可以顺利流下、防止稀硫酸的体积对CO2体积测量造成的误差.
【结果处理】锥形瓶中放有样品 3.58g,向锥形瓶中滴入一定量的稀硫酸,生成的气体体积(已换算成标准状况下)与加入稀硫酸的体积关系如图所示
(3)样品中NaHCO3、Na2CO3的物质的量之比3:1
(4)实验所用硫酸的物质的量浓度是1mol/L
方案乙:某同学设计了另一种方案,其操作
(5)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg.用酒精灯对其充分加热,冷却后称得其总质量为cg.残留在蒸发皿中的固体是(填化学式)Na2CO3样品中NaHCO3的质量分数为$\frac{168(b-c)}{62(b-a)}$×100%(用含字母的代数式表示).
分析 【实验探究】:(1)锥形瓶中有生成的二氧化碳气体;
(2)导气管A的作用是平衡压强使液体顺利流下;
【结果处理】:(3)根据图象及反应方程式计算出硫酸的物质的量浓度;
(4)设出二者物质的量,然后根据生成的总的二氧化碳的物质的量及碳酸氢钠和碳酸钠的质量列式计算即可;
(5)碳酸氢钠加热分解生成碳酸钠、二氧化碳气体和水,据此判断残留在蒸发皿中的固体;碳酸氢钠加热分解生成碳酸钠、二氧化碳气体和水,书写化学方程式;根据差量法计算出样品中碳酸氢钠的质量、碳酸氢钠的质量分数.
解答 解:【实验探究】:(1)锥形瓶中有生成的二氧化碳气体,充分反应后,针筒中气体读数为V mL,则反应中生成的CO2气体体积>Vml,
故答案为:>;
(2)导气管A的作用是平衡分液漏斗内和锥形瓶中气体压强,使得溶液可以顺利流下、防止稀硫酸的体积对CO2体积测量造成的误差,
故答案为:平衡分液漏斗内和锥形瓶中气体压强,使得溶液可以顺利流下、防止稀硫酸的体积对CO2体积测量造成的误差;
【结果处理】:(3)设碳酸氢钠物质的量为xmol,碳酸钠物质的量为y,由图象可知,消耗硫酸20mL,生成标况下的二氧化碳体积896mL,二氧化碳的物质的量为:$\frac{0.896L}{22.4L/mol}$=0.04mol,
根据二氧化碳物质的量列式:x+y=0.04,
根据质量关系列式:84x+106y=3.58
解得:x=0.03,y=0.01,
x:y=0.03:0.01=3:1,
故答案为:3:1;
(4)设硫酸溶液的体积为浓度为xmol/L,由图象可知,消耗硫酸20mL,生成标况下的二氧化碳体积896mL,二氧化碳的物质的量为:$\frac{0.896L}{22.4L/mol}$=0.04mol,
根据反应:HCO3-+H+=H2O+CO2
1mol 1mol
2x×0.02 0.04
列式:1mol×0.04=2x×0.02×1mol
解得x=1mol/L,
故答案为:1mol/L;
(5)碳酸氢钠加热发生的反应方程式为:2NaHO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,所以残留在蒸发皿中的固体为碳酸钠,
根据差量法:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O△m
168 62
m(NaHCO3) (b-c)g
样品中含有碳酸氢钠的质量为:m(NaHCO3)=$\frac{168(b-c)}{62}$g,此样品中NaHCO3的质量分数=$\frac{\frac{168(b-c)}{62}g}{(b-a)g}$×100%=$\frac{168(b-c)}{62(b-a)}$×100%
故答案为:Na2CO3;$\frac{168(b-c)}{62(b-a)}$×100%.
点评 本题考查了物质性质实验方案的设计,题目难度中等,正确理解题干信息为解答关键,注意掌握物质性质实验方案的设计原则,试题侧重考查学生的分析、理解能力及化学计算、化学实验能力.

| A. | Mg3N2与盐酸反应能生成两种盐 | B. | CaC2的水解产物是Ca(OH)2和C2H2 | ||
| C. | Si3N4的水解产物之一是H2SiO3 | D. | PCl5的水解产物是HClO和PH3 |
| A. | 甲元素的相对原子质量一定是$\frac{12a}{b}$ | |
| B. | 该甲原子的摩尔质量是aNAg | |
| C. | Wg该甲原子的物质的量一定是Wa/(NA)mol | |
| D. | Wg该甲原子所含质子数是10W/a |
| A. | Na2O、Na2O2为相同元素组成的金属氧化物,其中Na2O2不属于碱性氧化物 | |
| B. | SiO2是硅酸的酸酐,NO2是HNO3的酸酐 | |
| C. | Fe(OH)3与氢碘酸反应的类型为复分解反应 | |
| D. | 将Fe(OH)3胶体和泥水分别进行过滤,分散质均不能通过滤纸孔隙 |
①CH3CH2CH2CH2CH3
②
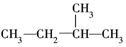
③
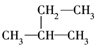
④
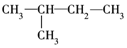
⑤
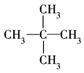
这些结构中出现重复的是( )
| A. | ②和③ | B. | ④和⑤ | C. | ③和⑤ | D. | 均不重复 |
| A. | 分液、萃取、蒸馏、蒸发 | B. | 萃取、蒸馏、分液、过滤 | ||
| C. | 分液、蒸馏、萃取、过滤 | D. | 蒸馏、萃取、分液、过滤 |
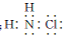 .
.



