6.在铝制易拉罐中收集满CO2,加入过量的NaOH溶液,立即封口并振荡,可以发现罐先咔咔作响,变瘪,然后再次鼓起来,其过程中没有涉及到的化学反应是( )
| A. | Al(OH)3分解 | B. | CO2+OH- | C. | Al+OH-+H2O | D. | Al2O3+OH- |
5.在某温度下,一密闭容器中模拟工业合成氨:N2(g)+3H2(g)?2NH3(g)△H<0;反应起始各物质的量如表:
达到平衡之后的 H2转化率α,NH3的体积分数为x%,下列说法错误的是( )
| N2 | H2 | NH3 | |
| 起始物质的量(mol) | 2 | 2 | 0 |
| A. | 平衡时NH3的物质的量:0mol<n(NH3)<$\frac{4}{3}$mol | |
| B. | 平衡时,N2的转化率为$\frac{α}{3}$ | |
| C. | 现将容器体积压缩到原来的一半,再次到达平衡之后,N2的体积分数变小 | |
| D. | 其他条件不变,若起始充入 N2、H2、NH3的物质的分别为:1.5mol、0.5mol、1mol,则到达平衡时,NH3的体积分数为x% |
4.关于溶液,下列说法正确的是( )
| A. | 0.1mol/L的NaHA其PH=1,溶液中存在:c(Na+)+c(H+)=c(OH-)+2c(A2-)+c(HA-) | |
| B. | 40%的醋酸溶液(p=1.049gcm-3)与60%的醋酸溶液(p=1.064gcm-3)等体积混合后,所得溶液中溶质的质量分数大于50% | |
| C. | 0.1mol/L的醋酸溶液V1L和等浓度的氢氧化钠溶液V2L混合后呈碱性,则一定有V1≤V2 | |
| D. | 1L0.5mol/LFeCl3的溶液与0.2L1mol/LKCl溶液中Cl-数目之比为15:2 |
3.下列叙述不正确的是( )
| A. | 在镀件上电镀铜时,可用金属铜作阳极 | |
| B. | 镀层破损后,白铁(镀锌)比马口铁(镀锡)更易被腐蚀 | |
| C. | 工业上电解饱和食盐水制烧碱,NaOH在阴极产生 | |
| D. | 钢铁在发生析氢腐蚀和吸氧腐蚀时,完全相同的反应是负极反应 |
2.下列说法正确的是( )
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由C(金刚石)→C(石墨)△H=-1.9KJ/mol 可知,金刚石比石墨稳定 | |
| C. | 在101Kpa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=+285.8KJ/mol | |
| D. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-53.7KJ/mol,若将含1 mol CH3COOH与含1 mol NaOH的溶液混合,放出的热量小于53.7KJ |
1.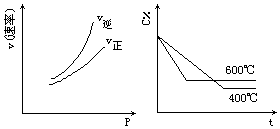 都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
 都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )| A. | N2O3(g)?NO2(g)+NO(g)-Q | B. | 3NO2(g)+H2O(l)?2HNO3 (aq)+NO(g)+Q | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+Q | D. | CO2(g)+C(s)?2CO(g)-Q |
20.关于下列各装置图的叙述不正确的是( )
| A. | 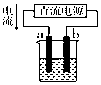 用装置精炼铜,则b极为精铜,电解质溶液为CuSO4溶液 | |
| B. | 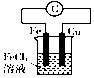 装置的总反应是Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 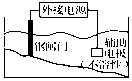 装置中钢闸门应与外接电源的负极相连 | |
| D. | 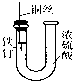 装置中的铁钉浸入浓硫酸中几乎没被腐蚀 |
19.下列各组离子能大量共存,且加入(或通入)X试剂后发生反应的离子方程式书写正确的是( )
| 选项 | 离子组 | X试剂 | 离子方程式 |
| A | Fe2+、Na+、SO42-、Cl- | 碘水 | 2Fe2++I2═2Fe3++2I- |
| B | pH=8的溶液中:Na+、HCO3-、Cl- | 少量澄清石灰水 | Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- |
| C | 透明溶液中:NH4+、Fe3+、Cl-、AlO2- | 过量铜粉 | Cu+2Fe═2Fe2++Cu2+ |
| D | K+、Na+、SO42-、ClO- | 少量SO2 | 2Cl-+SO2+H2O═2HClO+SO32- |
| A. | A | B. | B | C. | C | D. | D |
18.下列除去杂质的实验方法不正确的是( )
| A. | 除去Cl2中少量HC1气体:通过饱和食盐水后再干燥气体 | |
| B. | 除去Na2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| C. | 除去Fe(OH)3胶体中溶有的少量NaCl:加入适量水后过滤 | |
| D. | 除去CuCl2溶液中少量的FeCl3:加入稍过量的CuO后过滤 |
17. 用零价铁(Fe)去除水体中的硝酸盐(NO3- )已成为环境修复研究的热点之一.
用零价铁(Fe)去除水体中的硝酸盐(NO3- )已成为环境修复研究的热点之一.
(1)Fe 还原水体中NO3- 的反应原理如图所示.
①作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经 24 小时测 定NO3- 的去除率和 pH,结果如下:
pH 由 2.5 变为 4.5 时,NO3- 的去除率低,是因为生成了较多的不导电的FeO(OH),写出生成FeO(OH)的离子方程式:Fe3++2H2O?FeO(OH)+3H+.
(3)实验发现:在初始 pH=4.5 的水体中投入足量铁粉的同时,补充一定量的 Fe2+可以明显提高NO3- 的去除率.是因为 Fe2+能够破坏FeO(OH),氧化层生成Fe2O3.写出该反应的离子方式Fe2++2FeO(OH)=Fe3O4+2H+.
0 161229 161237 161243 161247 161253 161255 161259 161265 161267 161273 161279 161283 161285 161289 161295 161297 161303 161307 161309 161313 161315 161319 161321 161323 161324 161325 161327 161328 161329 161331 161333 161337 161339 161343 161345 161349 161355 161357 161363 161367 161369 161373 161379 161385 161387 161393 161397 161399 161405 161409 161415 161423 203614
 用零价铁(Fe)去除水体中的硝酸盐(NO3- )已成为环境修复研究的热点之一.
用零价铁(Fe)去除水体中的硝酸盐(NO3- )已成为环境修复研究的热点之一.(1)Fe 还原水体中NO3- 的反应原理如图所示.
①作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经 24 小时测 定NO3- 的去除率和 pH,结果如下:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 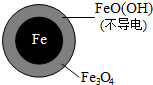 |  |
(3)实验发现:在初始 pH=4.5 的水体中投入足量铁粉的同时,补充一定量的 Fe2+可以明显提高NO3- 的去除率.是因为 Fe2+能够破坏FeO(OH),氧化层生成Fe2O3.写出该反应的离子方式Fe2++2FeO(OH)=Fe3O4+2H+.