题目内容
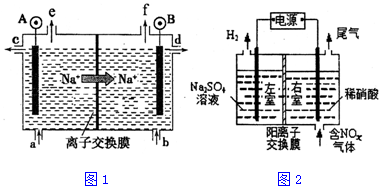
3.下列叙述不正确的是( )| A. | 在镀件上电镀铜时,可用金属铜作阳极 | |
| B. | 镀层破损后,白铁(镀锌)比马口铁(镀锡)更易被腐蚀 | |
| C. | 工业上电解饱和食盐水制烧碱,NaOH在阴极产生 | |
| D. | 钢铁在发生析氢腐蚀和吸氧腐蚀时,完全相同的反应是负极反应 |
分析 A、在镀件上镀铜时,镀层金属作阳极;
B、在原电池中,活泼金属做负极,负极金属更易腐蚀,正极金属被保护;
C、根据电解质中离子的放电顺序结合电解原理来回答;
D、钢铁在发生析氢腐蚀和吸氧腐蚀时,负极均是金属铁失电子的氧化反应.
解答 解:A.在镀件上镀铜时,镀层金属作阳极,所以可用金属铜作阳极,故A正确;
B.白铁(镀锌的铁)中,镀层破损后,Zn为负极,被腐蚀的是Zn,Fe被保护,马口铁(镀锡的铁)中,Fe为负极,被腐蚀的是Fe,Zn被保护,所以镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)铁更耐腐蚀,故B错误;
C.电解饱和食盐水制烧碱,在阴极上是氢离子得电子,氢氧根离子浓度增大,所以在阴极区产生NaOH溶液,故C正确;
D.钢铁在发生析氢腐蚀和吸氧腐蚀时,负极均是金属铁失电子的氧化反应,故D正确.
故选B.
点评 本题是一道综合知识题目,考查学生对原电池原理的应用知识,可以根据所学知识进行回答,注意原电池原理的应用是解题的关键,难度不大.

练习册系列答案
相关题目
13.下列叙述中正确的是( )
| A. | 1molO2的质量是32g•mol-1 | |
| B. | SO 42-的摩尔质量为 96 g•mol-1 | |
| C. | 1mol 任何物质的质量等于该物质的相对分子质量 | |
| D. | CO2的摩尔质量是44g |
14.光导纤维的主要成分是SiO2,下列关于SiO2的有关叙述正确的是( )
| A. | SiO2是酸性氧化物,它不溶于水也不溶于任何酸 | |
| B. | SiO2是制造玻璃的主要原料之一,它在常温下不与NaOH溶液反应 | |
| C. | 因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强 | |
| D. | CO2通入水玻璃中可得硅酸 |
18.下列除去杂质的实验方法不正确的是( )
| A. | 除去Cl2中少量HC1气体:通过饱和食盐水后再干燥气体 | |
| B. | 除去Na2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| C. | 除去Fe(OH)3胶体中溶有的少量NaCl:加入适量水后过滤 | |
| D. | 除去CuCl2溶液中少量的FeCl3:加入稍过量的CuO后过滤 |
8.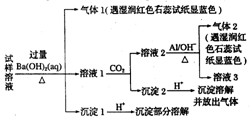 最近一段时间,武邑中学雾霾严重,影响了同学们的生活和健康.雾霾中可能含有如下离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.高三1490班某同学收集了操场的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验,根据实验操作与现象,该同学得出的结论不正确的是( )【已知:3NO3-+8Al+5OH-+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$3NH3↑+8AlO2-】
最近一段时间,武邑中学雾霾严重,影响了同学们的生活和健康.雾霾中可能含有如下离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.高三1490班某同学收集了操场的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验,根据实验操作与现象,该同学得出的结论不正确的是( )【已知:3NO3-+8Al+5OH-+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$3NH3↑+8AlO2-】
 最近一段时间,武邑中学雾霾严重,影响了同学们的生活和健康.雾霾中可能含有如下离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.高三1490班某同学收集了操场的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验,根据实验操作与现象,该同学得出的结论不正确的是( )【已知:3NO3-+8Al+5OH-+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$3NH3↑+8AlO2-】
最近一段时间,武邑中学雾霾严重,影响了同学们的生活和健康.雾霾中可能含有如下离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.高三1490班某同学收集了操场的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验,根据实验操作与现象,该同学得出的结论不正确的是( )【已知:3NO3-+8Al+5OH-+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$3NH3↑+8AlO2-】| A. | 试样中一定存在的阴离子是SO42-和NO3- | |
| B. | 试样中一定不含Al3+ | |
| C. | 该雾霾中可能存在NaNO3、NH4Cl和MgSO4 | |
| D. | 试样中可能存在Na+、Cl- |
15.下列图象正确的是( )
| A. | 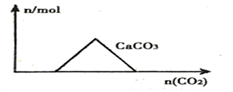 向Ca(OH)2和NaOH的混合溶液中通入CO2 | |
| B. | 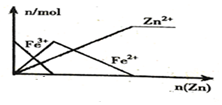 向FeCl3溶液中加入锌粉 | |
| C. | 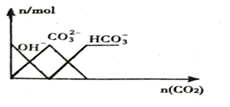 向NaOH溶液中通入CO2 | |
| D. | 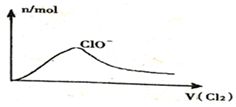 Cl2通入NaOH溶液中 |
12.下列物质的电子式书写正确的是( )
| A. | 次氯酸的电子式 | B. | 氟化氢的电子式: | C. | OH- | D. |  |