题目内容
6.在铝制易拉罐中收集满CO2,加入过量的NaOH溶液,立即封口并振荡,可以发现罐先咔咔作响,变瘪,然后再次鼓起来,其过程中没有涉及到的化学反应是( )| A. | Al(OH)3分解 | B. | CO2+OH- | C. | Al+OH-+H2O | D. | Al2O3+OH- |
分析 二氧化碳能与NaOH溶液反应,使罐内气体减少,压强减小,易拉罐变瘪,化学方程式为:CO2+2NaOH=Na2CO3+H2O;因加入过量的NaOH溶液,先铝制易拉罐表面的氧化铝反应,再与铝单质反应,由此分析解答.
解答 解:二氧化碳能与NaOH溶液反应,使罐内气体减少,压强减小,易拉罐变瘪,化学方程式为:CO2+2NaOH=Na2CO3+H2O;因加入过量的NaOH溶液,先铝制易拉罐表面的氧化铝反应,再与铝单质反应,所以涉及的离子反应依次有二氧化碳与氢氧化钠反应、氧化铝与氢氧化钠反应、铝与氢氧化钠溶液反应,没有涉及氢氧化铝的分解,
故选A.
点评 二氧化碳能与NaOH溶液反应,使罐内气体减少,压强减小,易拉罐变瘪,化学方程式为:CO2+2NaOH=Na2CO3+H2O;因加入过量的NaOH溶液,先铝制易拉罐表面的氧化铝反应,再与铝单质反应,

练习册系列答案
相关题目
17.在盛放浓硫酸的试剂瓶标签上应该印有下列警示标记中的( )
| A. |  爆炸品 | B. |  易燃液体 | C. |  剧毒品 | D. |  腐蚀品 |
1.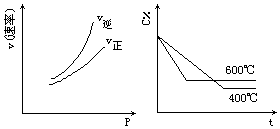 都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
 都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )| A. | N2O3(g)?NO2(g)+NO(g)-Q | B. | 3NO2(g)+H2O(l)?2HNO3 (aq)+NO(g)+Q | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+Q | D. | CO2(g)+C(s)?2CO(g)-Q |
11.下列对有机物结构或性质的描述,错误的是( )
| A. | 苯分子中的6个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间独特的键 | |
| B. | 将溴水加入苯中,溴水的颜色变浅,这是由于发生了加成反应 | |
| C. | 乙烷和丙烯的物质的最共1mol,完全燃烧后生成3molH2O | |
| D. | 主链上有5个碳原子的庚烷有5 种同分异构体 |
18.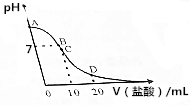 25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )
25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )
 25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )
25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )| A. | 在A点处的溶液中pH<12 | B. | 在B点:c(NH4+)=c(Cl-)>c(OH-)>c(H+) | ||
| C. | 在C点:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D. | 在D点:c(NH4+)+c(NH3•H2O)=2c(Cl-) |
15.硅是信息高速公路的基石,通常以硅石(SiO2>99.0%、还有少量的Al2O3、Fe2O3等)为主要原料制备,主要流程如图所示.
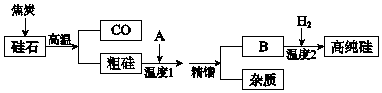
(1)从硅石中得到粗硅的化学方程式是SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,粗硅含有的杂质有铝、铁等.
(2)二氧化硅与焦炭在高温下也能得到一种硬度仅次于金刚石的物质金刚砂(化学式为SiC,Si为+4价),原理是SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑,该反应中的氧化剂是碳.
(3)若A是氯气,B是四氯化硅,精馏得到纯净SiCl4,温度应控制的范围是a(填序号).
a.55~60℃b.180~200℃c.300~320℃
则精馏分离出的杂质成分是FeCl3、AlCl3.
(4)若A是HCl,B是SiHCl3,生产过程中可循环利用的物质是HCl.

(1)从硅石中得到粗硅的化学方程式是SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,粗硅含有的杂质有铝、铁等.
(2)二氧化硅与焦炭在高温下也能得到一种硬度仅次于金刚石的物质金刚砂(化学式为SiC,Si为+4价),原理是SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑,该反应中的氧化剂是碳.
(3)若A是氯气,B是四氯化硅,精馏得到纯净SiCl4,温度应控制的范围是a(填序号).
| 物质 | SiCl4 | SiHCl3 | FeCl3 | AlCl3 |
| 熔点/℃ | -70 | -128.2 | 306 | -- |
| 沸点/℃ | 57.6 | 31.85 | 315 | 181 升华 |
则精馏分离出的杂质成分是FeCl3、AlCl3.
(4)若A是HCl,B是SiHCl3,生产过程中可循环利用的物质是HCl.