9.自然界中含量最多的金属元素和非金属元素形成的稳定化合物是( )
| A. | Al2O3 | B. | SiO2 | C. | Fe2O2 | D. | CaO |
8.由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是( )
| 选项 | 反应类型 | 反应条件 |
| A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
| B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
| C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
| D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
| A. | A | B. | B | C. | C | D. | D |
7.X、Y、Z、R、W是原子序数依次增大的短周期主族元素,它们原子的最外层电子数之和为22.X与Z同主族,Y与W同主族,R最外层电子数是电子层数的2倍.下列说法正确的是( )
| A. | 原子半径:W>R>Z | |
| B. | R的最高价氧化物的水化物酸性比W的强 | |
| C. | 气态氢化物的热稳定性:Y>W>R | |
| D. | W与X形成的是离子化合物 |
6.海水淡化是海岛地区提供淡水的重要手段,所谓海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),其方法较多,如水合物法、电渗透法、离子交换法和压渗法等.下列方法中也可以用来进行海水淡化的是( )
| A. | 过滤法 | B. | 蒸馏法 | C. | 萃取法 | D. | 结晶法 |
5.下列离子方程式正确的是( )
| A. | 铁与FeCl3溶液反应:Fe+Fe3+═2Fe2+ | |
| B. | Fe与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | FeCl2溶液与Cl2反应:Fe2++Cl2═Fe3++2Cl- | |
| D. | Fe(OH)3与盐酸反应:Fe(OH)3+3H+═Fe3++3H2O |
2.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( )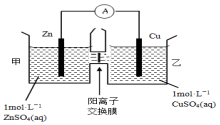

| A. | 铜电极上发生还原反应 | |
| B. | 电池工作一段时间后,甲池的c(SO42-)不变 | |
| C. | 电池工作一段时间后,乙池溶液的总质量增加 | |
| D. | 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
1.常温下,下列各组离子在相应的条件下可能大量共存的是( )
0 161204 161212 161218 161222 161228 161230 161234 161240 161242 161248 161254 161258 161260 161264 161270 161272 161278 161282 161284 161288 161290 161294 161296 161298 161299 161300 161302 161303 161304 161306 161308 161312 161314 161318 161320 161324 161330 161332 161338 161342 161344 161348 161354 161360 161362 161368 161372 161374 161380 161384 161390 161398 203614
| A. | pH=2的溶液中:S2O32-、K+、Cl-、Na+ | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=10-10 mol/L的溶液中:Na+、HCO3-、Cl-、K+ | |
| C. | 在$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3- | |
| D. | 由水电离产生的c(OH-)=1×10-12mol/L的溶液中:NO3-、Mg2+、Na+、SO42- |
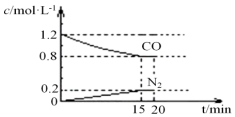 研究NOx、SO2、CO等大气污染气体的处理具有重要意义.
研究NOx、SO2、CO等大气污染气体的处理具有重要意义.